
题目列表(包括答案和解析)
1、美国等国家发射的航天器将我国研制的磁谱仪带入太空,其目的是探索反物质。反物质的主要特征是电子带正电荷,质子带负电荷。以下表示反物质酸碱中和反应的通式是 ( )
A、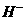 +
+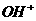 ==H2O
B、
==H2O
B、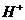 +
+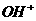 == H2O
== H2O
C、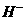 +
+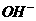 == H2O
D、
== H2O
D、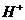 +
+ 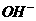 == H2O
== H2O
28.美国《科学美国人》杂志在1971年7月刊登的“地球的能量资源”一文中提供了如下数据:
到达地球表面的太阳辐射能的几条主要去路
|
直接反射 |
52,000×109 kJ·s-1 |
|
以热能方式离开地球 |
81,000×109 kJ·s-1 |
|
水循环 |
40,000×109 kJ·s-1 |
|
大气流动 |
370×109 kJ·s-1 |
|
光合作用 |
40×109 kJ·s-1 |
请选用以上数据计算:
(1)地球对太阳能的利用率约为 。
(2)通过光合作用,每年有 千焦的太阳能转化为化学能(每年按365天计)。
[解析] 地球对太阳能利用率包括水循环、大气流动、光合作用三部分。
[答案] (1)23.3% (2)1.26×1018
27.用浓氨水与氯气反应,其化学方程式为3Cl2+8NH3====6NH4Cl+N2。
(1)标出电子转移的方向和数目。
(2)当有160.5 g NH4Cl产生时,被氧化的氨气是多少克?
[答案]
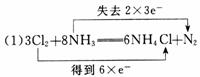
(2)17 g
26.有A、B、C、D四种可溶性离子化合物,它们的阳离子是Ag+、Na+、Mg2+、Cu2+,阴离子是Cl-、OH-、NO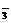 、SO
、SO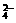 (每种离子只能用一次),现将溶液两两混合,记录现象如下:
(每种离子只能用一次),现将溶液两两混合,记录现象如下:
A+B 白色沉淀,A+C
白色沉淀,A+C 白色沉淀
白色沉淀
B+D 白色沉淀,A+D
白色沉淀,A+D 白色沉淀
白色沉淀
C+D 蓝色沉淀。已知Ag2SO4是微溶性白色沉淀,则A、B、C、D的化学式分别是 、
、 、
。
蓝色沉淀。已知Ag2SO4是微溶性白色沉淀,则A、B、C、D的化学式分别是 、
、 、
。
[解析]
首先考虑离子间的共存情况。Ag+与Cl-、OH-、SO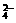 都产生沉淀,故只能与NO
都产生沉淀,故只能与NO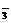 组合成AgNO3;Mg2+、Cu2+都不能与OH-共存,则OH-只能与Na+组合成NaOH;余Cl-、SO
组合成AgNO3;Mg2+、Cu2+都不能与OH-共存,则OH-只能与Na+组合成NaOH;余Cl-、SO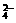 与Mg2+、Cu2+组合。
与Mg2+、Cu2+组合。
因A能与B、C、D都产生白色沉淀,说明A是AgNO3,NaOH虽也能与其他三种溶液产生沉淀,但Cu(OH)2是蓝色的。
C+D 蓝色沉淀,说明C与D的组合是NaOH与Cu2+反应。若C是NaOH,D是Cu2+,则B是Mg2+,因B与A产生沉淀,B应为MgCl2,D应是CuSO4,B+D就无法产生沉淀。若D是NaOH,C是Cu2+,则B应为MgCl2,C是CuSO4,B+D
蓝色沉淀,说明C与D的组合是NaOH与Cu2+反应。若C是NaOH,D是Cu2+,则B是Mg2+,因B与A产生沉淀,B应为MgCl2,D应是CuSO4,B+D就无法产生沉淀。若D是NaOH,C是Cu2+,则B应为MgCl2,C是CuSO4,B+D Mg(OH)2↓。经验证此情况符合条件。
Mg(OH)2↓。经验证此情况符合条件。
[答案] AgNO3 MgCl2 CuSO4 NaOH
25.某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO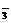 六种离子。
六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是 、 、 。
乙厂的废水中含有另外三种离子是 、 、 。
有一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的 (填写离子符号)转化为沉淀。经过滤后的废水主要含 ,可用来浇灌农田。
[解析] 本题旨在考查学生对离子反应、离子共存掌握的情况,可以看作是对“离子共存”的变体考查。同时兼顾对解决日常生产实际中问题的能力考查。
甲厂废水明显呈碱性,说明含有大量OH-,则Ag+、Fe3+因与之反应而不能共存,阳离子只可能含有K+,另一种离子尚须待定。
乙厂中含有另外三种离子,结合甲中分析,一定含有Ag+、Fe3+,而Ag+与Cl-不能大量共存,故阴离子只可能是NO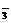 ,故Cl-属于甲厂废水中。
,故Cl-属于甲厂废水中。
甲乙两厂的废水按适当比例混合,因Ag+与Cl-、Fe3+与OH-反应转化为沉淀而滤去,故余KNO3(钾肥、氮肥)作为化肥可用来浇灌农田。
[答案] 甲:OH- K+ Cl-
乙:Ag+ Fe3+ NO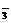
Ag+与Cl-、Fe3+与OH- K+、NO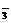 (或KNO3)
(或KNO3)
24.请设计一个只用BaCl2溶液及试管鉴别Na2CO3溶液和稀H2SO4的实验,简要写出鉴别过程和实验结论。
[解析] BaCl2都能跟Na2CO3、H2SO4反应产生白色沉淀,靠此是无法鉴别的。但题目要求只用BaCl2溶液,暗示反应后可能有办法。
因BaCl2+H2SO4====BaSO4↓+2HCl
而BaCO3沉淀能溶解于稀盐酸中,靠此可以鉴别。
[答案] 取两种待鉴溶液于两支试管中,分别滴加BaCl2试剂,都产生白色沉淀,静止,待沉淀沉于管底后,倒出各自的上层清液,分别滴加到另一支试管里的沉淀中,看沉淀是否溶解,溶解者为BaCO3沉淀,则该试管原盛试剂是Na2CO3。
Ba2++CO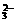 ====BaCO3↓
====BaCO3↓
BaCO3+2H+====Ba2++CO2↑+H2O
Ba2++SO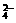 ====BaSO4↓
====BaSO4↓
23.除去下列物质中的杂质(括号内),写出选用的试剂及反应的离子方程式。
(1)NaCl(Na2CO3)
(2)Na2CO3(NaOH)
(3)CaCl2(CaCO3)
(4)Cu(Fe)
[答案] (1)HCl CO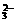 +2H+====CO2↑+H2O
+2H+====CO2↑+H2O
(2)CO2 CO2+2OH-====CO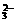 +H2O
+H2O
(3)HCl CaCO3+2H+====Ca2++CO2↑+H2O
(4)HCl Fe+2H+====Fe2++H2↑
22.用下列方法制取氧气,正确的操作顺序的序号是
①加热,用排水法收集一试管氧气
②称取1.2 g KClO3与制得的CuO粉末混合均匀后,装入大试管,用带有导管的单孔橡胶塞塞紧。
③装配好实验装置,检查装置的气密性。
④撤出导气管。
⑤停止加热。
⑥用带火星的木条伸入试管中检验收集的氧气。
[答案] ③②①④⑤⑥
21.(1)在烧杯或试管里进行固体物质的溶解时,为了加快溶解速度,常采用的方法有 、 、 。
(2)假设液体的刻度在滴定管的位置是20 mL(此滴定管规格是50 mL),全放出后,液体的体积是30 mL吗,为什么?
[答案] (1)粉碎固体 加热 搅拌或振荡等
(2)体积大于30 mL,因为“50 mL”刻度下还有一段无刻度。
20.用托盘天平称得某物质的质量为6.5 g。如果发现砝码和固体物质的位置放反了,则该物质的实际质量是
A.5.5 g B.7 g C.6 g D.7.5 g
[答案] A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com