
题目列表(包括答案和解析)
6.下列叙述正确的是
A.1 mol H2O的质量为18g/mol B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g D.标准状况下,1 mol任何物质体积均为22.4L
5.过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤
正确的操作顺序是
A.③②①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
4.实验中的下列操作正确的是
A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.Ba(NO3)2 溶于水,可将含有Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道
C.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
3.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是




A B C D
2.下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
1.如果你家里的食用花生油混有水份,你将采用下列何种方法分离
A.过滤 B.蒸馏 C.分液 D.萃取
X元素位于第ⅡA族,核内有12个中子,它在最高价的氧化物中的质量分数是60%。Y元素的原子核外有17个电子。X与Y所形成的化合物的化学式为 ,它是通过 结合的。用电子式表明其形成过程
.
14、(12分)原子序数为114号的稳定同位素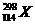 预测。
预测。
(1)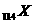 元素位于元素周期表第
周期 族,为 元素(“金属”、“非金属”)。
元素位于元素周期表第
周期 族,为 元素(“金属”、“非金属”)。
(2)其最高价氧化物及其对应水化物的分子式分别是 、 、 (用含X的式子表示),并估计后者为 性(“酸”、“碱”、“两”)。
(3)它与氯生成化合物的分子式 、 (用含X的分子式表示).
13、(10分)用电子式表示下列物质的结构:
①Ca(OH)2 ②H2O
③NH3 ④CS2
12、(12分)请根据元素周期律和元素周期表回答以下问题。
(1)下列叙述中,正确的是………………………………………..( )
A、室温时,0族元素的单质都是气体
B、同周期元素中,ⅦA族元素的原子半径最大
C、ⅥA族元素的原子,其半径越大,越容易得到电子
D、元素周期表中从ⅢB到ⅡB族这10个纵列的元素都是金属元素
|
X |
Y |
|
|
|
Z |
W |
(2)X、Y、Z均为短周期元素,它们在元素周期表中的位置
如右图所示。若Y原子的最外层电子数是此外层电子数的3倍,
下列说法正确的是 ……………………………( )
A、原子半径: W>Z>Y>X
B、W的单质能与水反应,生成一种具有漂白性的物质
C、四种元素的单质中,Z单质的熔沸点最高
D、最高价氧化物对应水化物的酸性:Z>W>X
(3)铊(Tl)位于元素周期表的ⅢA族.有的同学预测:单质铊能与盐酸反应放出氢气,氢氧化铊是两性氢氧化物.你认为这个同学的预测正确吗?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com