
题目列表(包括答案和解析)
4、需要加入氧化剂才能完成的变化的是 ( )

 A、CO2 HCO
A、CO2 HCO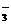 B、Fe2+ Fe3+
B、Fe2+ Fe3+

 C、Cl2 Cl-
D、KMnO4 MnO2
C、Cl2 Cl-
D、KMnO4 MnO2
3、下列反应中,盐酸作还原剂的是 ( )
A、NaOH + HCl = NaCl + H2O B、Zn + 2HCl = ZnCl2 + H2↑
C、H2 + Cl2 = 2HCl D、MnO2 + 4HCl = MnCl2 + 2H2O + Cl2↑
2、下列反应中,不是氧化还原反应的是 ( )
①H2+Cl2 2HCl ②Na2CO3+2HCl==2NaCl+H2O+CO2↑ ③2H2O
2HCl ②Na2CO3+2HCl==2NaCl+H2O+CO2↑ ③2H2O 2H2↑+O2↑
2H2↑+O2↑
④CuO+2HNO3==Cu(NO3)2+H2O ⑤2HgO 2Hg+O2↑
2Hg+O2↑
A. ②④ B. ①③ C. ①②③ D. ④⑤
1、下列说法正确的是 ( )
A、复分解反应可能是氧化还原反应
B、化合反应都不是氧化还原反应
C、分解反应不一定是氧化还原反应
D、没有单质参加或生成的反应一定是非氧化还原反应
16.(10分)常温下,在27.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21g /cm3,求:
① 该溶液中阴阳离子的总物质的量 ② 该溶液中CuSO4的物质的量浓度
③ 取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
15.(10分)甲乙两人分别用不同的方法配制100ml 3.6mol/L的稀硫酸。
(1)甲:量取20 ml 18 mol/L浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
① 实验所用的玻璃仪器除烧杯和容量瓶外,还有 ;
② 将溶液转移到容量瓶中的正确操作是
;
③ 定容的正确操作是
。
(2)乙:用100 ml 量筒量取20 ml 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 ml 刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处
。
14.(12分)
(1)CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别之(简要地写出实验过程)
① 只允许用一种试剂
② 不用任何试剂
(2)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是
13.(8分)如右图所示a、b、c、d分别是几种
常见漏斗的上部,A、B、C、D是实际操作中各漏
斗的下部插入容器中的示意图,请指出A、B、C、
D分别与a、b、c、d相匹配的组合及其组合后装置
在实验中的应用,例如:C和a组合,用于制取气
体。
① A与 组合,用于 ,② B与 组合,用于 ,
③ B与 组合,用于 ,④ D与 组合,用于 ,
12.0.5L 1mol/L FeCl3溶液与0.2L1mol/L KCl溶液中的Cl-的数目之比
A.5:2 B. 3:1 C.15:2 D. 1:3
11.欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是
① 将14.2 g Na2SO4 溶于100ml水中 ② 将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③ 将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A.①② B.②③ C.①③ D.①②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com