
题目列表(包括答案和解析)
6.下列各分子中所有原子都满足最外层为8电子结构的是( )(全国高考题)。
(A)光气(COCl2) (B)六氟化硫 (C)二氟化氙 (D)三氟化硼
5.下列分子中,属于含极性键的非极性分子的是( )(全国高考题)。
(A)H2O (B)Cl2 (C)NH3 (D)CCl4
4.据最新科技报导,科学家发现了新型氢微粒,这种微粒是由3个氢原子核(只含质子)和2个电子构成。对于这种微粒,下列说法中正确的是( )
A、是氢的一种同素异形体 B、是氢的一种新的同位素
C、它比一个普通H2分子多一个氢原子 D、它的组成可用H3+表示
3.下列气态氢化物中最稳定的是 ( )
A、PH3 B、H2O C、NH3 D、CH4
2.据最新科技报导,科学家发现了新型氢微粒,这种微粒是由3个氢原子核(只含质子)和2个电子构成。对于这种微粒,下列说法中正确的是( )
A、是氢的一种同素异形体 B、是氢的一种新的同位素
C、它比一个普通H2分子多一个氢原子 D、它的组成可用H3+表示
1.下列各组微粒,互称为同位素的是( )
A、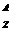 X和
X和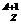 X B、
X B、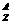 M和
M和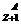 N C、
N C、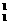 H+ 和D+ D、O2和O3
H+ 和D+ D、O2和O3
26.(7分)将2.000 g Na2SO4、Na2CO3和NaNO3的混合物溶于水得溶液A,在A中加入足量未知浓度的BaCl2溶液10.00 mL,然后过滤得沉淀B3.315g和滤液C;在C中加入足量的AgNO3溶液,又生成5.740 g沉淀;向B中加入足量稀硫酸,充分反应后,沉淀质量变为3.495g。计算:
⑴氯化钡溶液的物质的量浓度。
⑵原混合物中硝酸钠的质量分数。
⑴n(Cl-) = 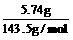 = 0.04 mol (1分)c(BaCl2) =
= 0.04 mol (1分)c(BaCl2) = 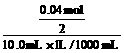 = 2.0 mol/L (1分)
= 2.0 mol/L (1分)
⑵Na2CO3 - BaCO3 - BaSO4 Δ m (1分)
1mol 197 g 233 g 36g
n(Na2CO3) =(3.495g-3.315g)÷36g·mol-1 = 0.005mol (1分)
n(Na2SO4) = (3.315g-0.005mol×197 g·mol-1) ÷233 g·mol-1= 0.01mol(1分)
m(NaNO3)=2.000g-0.005mol×106 g·mol-1- 0.01mol×142 g·mol-1= 0.05g(1分w(NaNO3)=0.050g÷2.000g=0.025(2.5%)(1分)
25.(12分)根据下图回答问题:
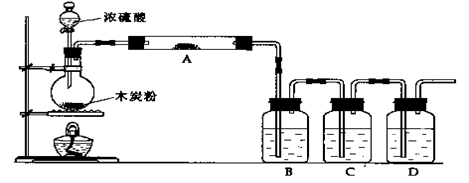
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气。
答:
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:_______________________________________________________________。
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是_______________________;作用是_______________________。
B中加入的试剂是_______________________;作用是_______________________。
C中加入的试剂是_______________________;作用是除尽________________气体。
D中加入的试剂是_______________________;作用是_______________________。
(4)实验时,C中应观察到的现象是_________________ __ ______________。
(1)反应前先用小火加热烧瓶,B、C、D瓶中有气泡冒出,停止加热后,水会升到导管里形成一段水柱,证明装置不漏气。
|
(2)2 H2SO4(浓)+C ===2H2O+2SO2↑+CO2↑
(3) A:无水硫酸铜 检验H2O B:品红溶液 检验SO2
C:酸性高锰酸钾溶液 检验SO2 D:澄清石灰水 检验CO2
(4)酸性KMnO4 溶液的颜色不褪尽(或不褪色,或不褪成无色)。
24.(9分)在实验室利用胆矾(CuSO4·5H20)晶体和烧碱溶液制备氧化铜固体,其实验操作可分解为如下几步:①混合 ②过滤 ③加热分解 ④溶解 ⑤洗涤。就此实验完成下列填空:
⑴正确操作步骤的顺序(填序号) ;
⑵步骤②中所用到的玻璃仪器有 ;
⑶在该实验中多次用到玻璃棒,其作用有三个,分别是 、 、 。
⑴ ④、①、③、②、⑤ (3分) ⑵ 玻璃棒、漏斗、烧杯 (3分)
⑶ 搅拌、引流、转移(3分)
23.(10分)有X、Y、Z三种短周期元素,X的气态氢化物化学式为H2X,此氢化物的式量与X最高价氧化物的式量之比为17∶ 40,X原子核内质子数与中子数相等,Y与X可以形成离子化合物Y2X,Y的阳离子电子层结构与Ne的相同,Z与X同周期,其气态单质是双原子分子,两原子共用1对电子。试回答:
(1)写出各元素符号:X 、Y 、Z 。
(2)X离子的结构示意图为 ;X与Y形成的离子化合物的电子式为 ,Z和氢形成的化合物的电子式为 。
(3)Y单质在空气中燃烧的化学方程式为 ,生成物与CO2反应的化学方程式为 。
(1)S,Na,Cl
(2)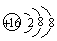 , Na+
, Na+ 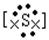 2- Na+,
2- Na+, 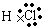 (3)2Na + O2
(3)2Na + O2 Na2O2,2Na2O2 + 2CO2
= 2 Na2CO3 +
O2
Na2O2,2Na2O2 + 2CO2
= 2 Na2CO3 +
O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com