
题目列表(包括答案和解析)
36.A、B、C、D四种短周期元素的原子序数依次增大。A、D同主族,B、C同周期。A、B组成 的化合物甲为气态,其中A、B原子数之比为4∶1。由A、C组成的两种化合物乙和丙都为液态 ,乙中A、C原子数之比为1∶1,丙中2∶1。由D、C组成的两种化合物丁和戊都为固态,丁中 D、C原子数之比为1∶1,戊中为2∶1。写出化学式,甲 ,
乙 ,丙 ,丁 ,戊 。
35.据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其极强的爆炸性,又称为“盐粒炸弹”。科学家发现“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排列成V形,如果5个N结合后都达到8电子结构,
且含有2个氮氮叁键,则“N5”分子碎片所
带电荷是____________,写出它的电子式:_______________________________________
在1999年曾报道合成和分离了含高能量正离子N的化合物 N5AsF6(N与As是同主族元素) ,
那么“N5”正离子共有 个核外电子,化合物N5AsF6中As化合价为 ,F化合价为 。
34.有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1)元素名称: A ________ B __________ C __________ D ___________
(2)写出AB2 的电子式为 ______________
(3)画出D的原子结构简图 ___________________, 用电子式表示化合物 C2D 的形成过程 _____________________________________。
33.已知LiH属于离子化合物,LiH与水反应可放出氢气,下列叙述中正确的是( )
A.LiH的水溶液呈酸性 B.LiH是一种强氧化剂
C.LiH中氢离子可被还原为氢气 D.LiH中氢离子与锂离子核外电子排布相同。
32.下列指定粒子的个数比为2∶1的是( )
A.Be2+离子中的质子和电子
B.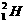 原子中的中子和质子
原子中的中子和质子
C.NaHCO3晶体中的阳离子和阴离子 D.BaO2(过氧化钡)固体中的阴离子和阳离子
31.下列各组指定原子序数的元素,不能形成AB2型化合物的是( )
A、6和8 B、16和8 C、12和9 D、11和16
30.下列各微粒的图或式表示正确的是 ( )
A.HClO结构式:H-O-Cl B.MgBr2电子式:Mg2+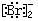
C.Al3+离子结构示意图: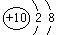 D.NH3电子式:
D.NH3电子式: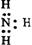
29.NA代表阿伏加德罗常数,下列说法不正确的是( )
A.16 g18O2中含的原子数为NA
B.在常温常压下,1mol氖气含有原子数为NA
C.1 mol H2O在标准状况下所占体积约为22.4 L
D.1 mol H2O2分解时,电子转移总数为NA
28.用NA表示阿佛加德罗常数, 下列叙述中正确的是( )
A、18 g 的H2O中含有NA 个质子
B、1/18 mol的1H35Cl分子所含中子数约为6.02×1023
C、3.5 g的35Cl2气体的体积为2.24 L
D、1 mol Fe 作为还原剂提供的电子数一定为 2NA
27.已知短周期元素的离子aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是:( )
A.元素的非金属性:A > B > D> C B.原子序数:d>c>b>a
C.离子半径:C3-> D-> B+> A2+ D.原子半径:B>A>C>D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com