
题目列表(包括答案和解析)
27、(5分)《实验六 同周期、同主族元素性质的递变》中有一段实验如下 :
取一块白色点滴板,在三个孔穴中分别滴入3滴NaCl溶液、NaBr溶液和NaI溶液,再向各孔穴中分别滴入2滴新制的氯水;再用溴水人替氯水在另三个孔穴中做上述实验。
根据以上实验填空回答。
(1)该实验的目的是___________________________________________________
(2)写出三个孔穴中发生反应的化学方程式
__________________________________,__________________________________
__________________________________。
(3)实验中为何要用新制的氯水____________________________________________
_____________________________________________________________________。
26、(5分)三位同学分别设计了下述3个实验方案以验证某无色气体中既含有二氧化硫又含有二氧化碳。 方案1:将无色气体通入酸性高锰酸钾溶液,高锰酸钾溶液褪色,反应的气体通入石灰水,石灰水变浑浊,即可证明原无色气体中既含有二氧化硫又含有二氧化碳 方案2:将无色气体通入溴水中,溴水褪色,反应的气体通入石灰水,石灰水变浑浊,即可证明原无色气体中既含有二氧化硫又含有二氧化碳 方案3:将无色气体通入品红溶液后再通入酸性高锰酸钾溶液最后通入石灰水,结果品红试液褪色,高锰酸钾溶液颜色稍变浅,石灰水变浑浊,即可证明原无色气体中既含有二氧化硫又含有二氧化碳 试回答:上述3个实验方案中,确实能证明原无色气体中既含有二氧化硫又含有二氧化碳的是实验方案是______。请简要说明你作出如此判断的理由 (按下列要求回答):
方案 的缺点是:______________________________________________
方案 的缺点是:______________________________________________ 。
25、(5分) 长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:
①称量a g样品,置于烧杯中。
②加入适量蒸馏水,使样品溶解。
③加入稀盐酸,使溶液呈强酸性,再加过量的BaCl2溶液。
④过滤,用蒸馏水洗涤沉淀。
⑤加热干燥沉淀物。
⑥将沉淀物冷却至室温后,称量。
⑦重复⑤、⑥操作直到合格,最后得到b g固体。
回答下面问题:
(1)本实验中是否能用Ba(NO3)2代替BaCl2? 。 其理由是: 。
(2)步骤③中加盐酸使溶液呈强酸性的目的是: 。
(3)步骤⑦的“合格”标准是: 。
(4)实验测得样品中无水亚硫酸钠的质量分数是:(列出算式,不需化简) 。
24、(8分)过氧化氢(H2O2)又称双氧水,常温下它是一种液体,难电离且易分解。作为一种经典化工产品,工业上早就在100多年前就开始生产它。随着社会需求的增长,尤其是生态环境保护的需要,过氧化氢近年来更受到人们的青睐,并称其为绿色氧化剂。
根据上述材料,回答下列问题:
(1)依据已有的知识,写出H2O2的结构式: 。
(2)H2O2可自行分解,但速度极慢。如果在3%的H2O2中加入新鲜的肝脏碎块,则立即有大量的气泡产生。写出产生气泡的有关化学反应方程式
(3)过氧化氢被称为绿色氧化剂的主要原因是
(4)久置的油画,白色部位(PbSO4)常会变黑(PbS),用双氧水揩擦后又恢复原貌,有关反应的化学方程式为 。
23、(4分)工业上硅是在电炉里用碳还原二氧化硅制得的写出该反应的化学方程式 ,若用30g二氧化硅与0.5mol碳反应,可制得硅 mol,在此反应氧化剂是 ,反应中转移的电子数是 。
22、(5分)近年来,科学家在氦的气氛中给石墨电极通电,石墨挥发,在其挥发的黑烟中发现了C60,C60的金属渗入物具有可贵的超导性质。北京大学首先将C60渗锡,获得超导转变温度为37K的好成绩,这种C60与石墨互为 ,其摩尔质量为 ,若要确证其元素组成,可将其在足量氧气中燃烧,再用 试剂来检验生成的 气体,现象是 。
21、(10分) 下面是元素周期表的一部分,针对①-⑩元素填写下列空白
|
主族 周期 |
IA |
|
O |
|||||
|
1 |
① |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
|
|
2 |
|
|
|
② |
|
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)在这些元素中,属于金属元素的有________________(填元素符号)
(2)画出⑦元素原子结构示意图______________________________
(3)写出①和⑩形成的化合物的电子式_______________________
(4)用电子式表示④和⑥形成化合物的过程_____________________
(5)写出①和②的最低价形成气态分子的化学式__________________。
(6)根据原子结构理论和元素周期律,请回答关于原子序数为113号元素(暂且用X代替其元素符号)几个问题:
①该元素位于元素周期表的位置是 ,属 元素(填金属或非金属元素);
②该元素的最高价氧化物对应水化物的化学式为 。
20、溴化碘(IBr)的结构和性质与Br2和I2相似,下列关于IBr的叙述中不正确的是( )
A.IBr是共价化合物 B.IBr跟水反应时,IBr既是氧化剂又是还原剂
C.IBr也能溶于NaOH溶液 D.IBr的电子式为 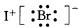
19、把浓硫酸滴入浓盐酸中,会有氯化氢气体逸出,对此现象的合理解释是( )
A.氯化氢难溶于水 B.浓硫酸有脱水性
C.浓硫酸是一种高沸点的酸 D.浓硫酸溶于水放出大量的热,降低了氯化氢的溶解度
18、下列各组物质间,不能发生反应的是( )
A、SiO2和CaO(高温) B、SiO2和NaOH溶液(常温)
C、SiO2和C(高温) D、SiO2和浓HNO3(常温)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com