
题目列表(包括答案和解析)
22.世界环保联盟即将全面禁止在自来水中加氯气(Cl2,黄绿色气体),推广采用光谱高效消毒剂二氧化氯,目前欧州和我国主采用Kesting法[原料为氯酸钠(NaClO3)与盐酸]制取ClO2,该法的缺点是同时会产生Cl2。该法制ClO2的化学方程式为
2NaClO3+4HCl == 2ClO2↑+Cl2↑+2NaCl+2H2O
(1)若生成0.1mol Cl2,转移的电子的物质的量为 ,该反应中氧化产物为 。
(2)盐酸在反应中显示出来的性质是:(填写编号) 。
①只有还原性 ②具有还原性与酸性 ③只有氧化性 ④具有氧化性和酸性
21.(1)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀时为止,
写出反应的离子方程式: 。
在以上溶液中,继续滴加NaHSO4溶液,写出反应的离子方程式:
。
(2) 按要求写出离子的反应方程式:
① CaCO3+( )== ( ) +CO2↑+H2O
②( )+OH-== H2O +CO32-
③ Al2O3 +( )== 2Al O 2- +H2O
20.18g某混合气体通过足量的Na2O2 固体,充分反应后固体增重2g,则该混合气体不可能是
A.H2O(g)、O2 B.CO2、H2O(g)
C.CO2、H2 D.CO2、H2O(g)、O2
第II卷 (共计50分)
19.已知 20mL 含有0.05mol/L的R2O72-溶液恰好能将20mL浓度为 0.3mol/L的Fe2+
完全氧化,则元素R在还原产物中的化合价为
A .+2价 B.+3价 C.+4价 D.+5价
18.V L浓度为0.5mol/L的盐酸,欲使其浓度增大一倍,采取的合理措施是
A.通入标准状况下的HCl气体11.2V L
B.加入10mol/L的盐酸0.1V L,再稀释至1.5V L
C.将溶液加热浓缩至0.5V L
D.加入V L1.5 mol/L的盐酸混合均匀
17.下列关于氧化钠和过氧化钠的叙述中,正确的是
A.都属于碱性氧化物 B.都能与水发生化合反应
C.水溶液的成分相同 D.与二氧化碳反应生成不同的盐
16.有下列氧化还原反应:
① Fe+CuSO4==Cu+FeSO4
② Cu+2FeCl3==CuCl2+2FeCl2
③ 2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O
④ 2FeCl2+Cl2==2FeCl3
根据上述反应可判断各粒子氧化性由强到弱的顺序正确的是
A.
MnO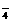 >Cl2>Fe3+>Cu2+>Fe2+
B. Cl2>MnO
>Cl2>Fe3+>Cu2+>Fe2+
B. Cl2>MnO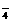 >Cu2+>Fe2+>Fe3+
>Cu2+>Fe2+>Fe3+
C.
MnO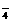 >Fe3+>Cu2+>Cl2>Fe2+ D. Fe3+>MnO
>Fe3+>Cu2+>Cl2>Fe2+ D. Fe3+>MnO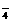 >Cl2>Cu2+>Fe2+
>Cl2>Cu2+>Fe2+
15. “可燃冰”的主要成分是甲烷与水分子(CH4·xH2O)。据测定每1 m3这种晶体可释放出140 m3的甲烷气体(假设气体体积已折算为标准状况,可燃冰的密度近似为1 g/cm3),试推算该“可燃冰”中,CH4与H2O分子个数比
A.1 :6 B.1 :7 C. 1 :8 D.1 :9
14.相同物质的量的KClO3分别发生下述反应:
①有MnO2 催化剂存在时,受热分解得到氧气;
②若不使用催化剂,加热至470℃左右,得到KClO4(高氯酸钾)和KCl。
下列关于①和②说法不正确的是
A.都属于氧化还原反应 B.发生还原反应的元素相同
C.发生氧化反应的元素不同 D.生成KCl的物质的量相同
13.NA代表阿伏加德罗常数,以下说法正确的是:
A.62g Na2O溶于水后,所得溶液中含有O2-数为NA
B.常温常压下,48 g O3含有的氧原子数为3NA
C.同温同压下,相同体积的任何气体单质所含的原子数相同
D.2.7 g金属铝变为铝离子时失去的电子数为 0.3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com