
题目列表(包括答案和解析)
18.在体积为VmL密度为ρg/cm3的溶液中,含有式量为M的溶质mg,其物质的量浓度为c mol/L,溶质质量分数为ω%,下列表示式中正确的是
A.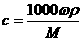 B.
B.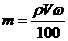 C.
C.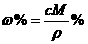 D.
D.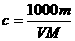
第Ⅱ卷(非选择题,共78分)
17.绝大多数盐类是强电解质,而醋酸铅是弱电解质。能证明醋酸是弱电解质的方法是
①比较相同浓度的醋酸铅和硫酸镁溶液的导电性 ②硫酸铅沉淀中加入醋酸铵,沉淀消失 ③测定醋酸铅的熔点 ④测定醋酸铅的溶解度
A.①② B.①③ C.②④ D.③④
16.甲、乙两烧杯中分别加入等体积、等浓度的稀H2SO4,向甲烧杯中加入m gMg,向乙烧杯中加入m gZn。待反应完毕后,一烧杯中仍有金属未溶解,则甲、乙烧杯中原来的H2SO4物质的量x值的取值范围是( )
A.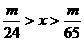 B.
B.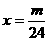
C.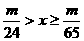 D.
D.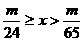
15.在一个量气管中充入1/4体积的N2、1/2体积的Cl2、1/4体积的H2,让日光照射一段时间后,倒立在水中,再让日光照射一段时间,则进入量气管中的水占量气管体积的
A.1/3 B.1/2 C. 5/8 D.3/8
14.下列离子方程式中,书写不正确的是 A.氯化钠溶液中加入硝酸银溶液:Ag+ + Cl-=AgCl↓ B.把金属钠放入水中:Na + 2H2O = Na+ +2OH-+ H2↑ C.将溴水加入碘化钾溶液中:Br2 + 2I-=2Br- + I2 D.盐酸滴在石灰石上:CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O
13.在酸性的无色透明溶液中,能大量共存的离子组是
A.Ba2+、Ag+、NO3-、Cl- B. K+、Cu2+、NO3-、MnO4-
C.HCO3-、K+、SO42-、Cl- D.Mg2+、NH4+、NO3-、Cl-
12.根据下列反应:(1)2Fe3++2I-=2Fe2++I2 ; (2)Br2+2Fe2+=2Br-+2Fe3+ 判断离子的还原性由强到弱的顺序是
A.Br->Fe2+>I- B. Fe2+>I->Br-
C.Br->I->Fe2+ D.I->Fe2+>Br-
11.下列各物质属于非电解质的是
①NaOH ②蔗糖 ③铜 ④Na2CO3 ⑤酒精 ⑥CaO
⑦CO2 ⑧醋酸 ⑨氯水 ⑩CaCO3
A.②③⑦⑩ B.②③⑤⑦ C.②⑤⑦ D.②⑦⑧⑨
10.下列叙述正确的是 A.1mol任何气体的体积一定是22.4L B.同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同 C.在标准状况下,体积为22.4L的物质都是1mol D.在非标准状况下,1mol任何气体的体积可能是22.4L
9.某密闭容器的质量为50.0g,当它装满CO2气体质量为58.8g,如果在同样条件下改为装满CH4气体,其质量应为
A.3.2g B.58.8g C.22.4g D.53.2g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com