
题目列表(包括答案和解析)
17.下列各反应的反应式或离子方程式中,能够说明次氯酸是弱电解质的是
A.次氯酸光照下分解:2HClO 2HCl+O2↑
2HCl+O2↑
B.次氯酸钙溶液中通入适量二氧化碳气体产生白色沉淀:
Ca(ClO)2+CO2+H2O====CaCO3↓+2HClO
C.次氯酸与氢氧化钠中和:HClO+NaOH====NaClO+H2O
D.次氯酸与H2SO3作用:HClO+H2SO3====H2SO4+HCl
[解析] 碳酸是弱酸,通入二氧化碳产生HClO,说明HClO更弱。
[答案] B
16.一个燃烧天然气(主要成分是甲烷CH4)的炉具,改成燃烧液化石油气(主要成分是C3H8等)的炉具,其改造办法是
A.增大进空气的孔,适当减小燃气出孔
B.增大燃气出孔,适当减小进空气的孔
C.适当减小进空气的孔,同时减小燃气出孔
D.适当减小进空气的孔,并增大燃气出孔
[解析] CH4、C3H8燃烧的反应方程式为:
CH4+2O2 CO2+2H2O
CO2+2H2O
C3H8+5O2 3CO2+4H2O
3CO2+4H2O
相同体积的CH4与C3H8完全燃烧,前者比后者需O2少。
[答案] A
15.在强碱溶液中,下列无色透明溶液中不可能大量共存的一组是
A.Na+、Cl-、Ba2+、NO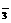 B.CO
B.CO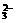 、Na+、Cl-、NO
、Na+、Cl-、NO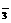
C.Na+、NO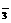 、K+、MnO
、K+、MnO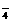 D.Mg2+、Al3+、Cl-、NO
D.Mg2+、Al3+、Cl-、NO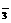
[解析] 强碱环境中存在大量OH-,阳离子Mg2+、Al3+均发生反应而不能大量共存;尽管在OH-环境下,MnO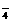 能与Na+、NO
能与Na+、NO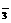 、K+共存,但MnO
、K+共存,但MnO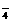 在溶液中呈紫红色,不合题意。
在溶液中呈紫红色,不合题意。
[答案] D
14.已知H2S是弱电解质,把反应:2FeCl3+H2S====2FeCl2+S↓+2HCl用离子方程式表示,正确的是
A.2Fe3++H2S====2Fe2++2H++S↓
B.Fe3++H2S====Fe2++2H++S↓
C.2Fe3++S2-====2Fe2++S↓
D.2Fe3++2Cl-+S2-+2H+====2Fe2++S↓+2HCl
[解析] FeCl3是强电解质,在溶液中能电离出Fe3+,H2S是弱电解质,只能写分子式,同时必须兼顾电荷守恒。
[答案] A
13.下列表示的离子方程式正确的是
A.NH4NO3溶液与氢氧化钠共热:H++OH-====H2O
B.NH3·H2O滴入AlCl3溶液产生沉淀:3OH-+Al3+====Al(OH)3↓
C.NaOH溶液与NaHCO3溶液混合:OH-+H+====H2O
D.Al(OH)3固体可溶于稀硫酸中:Al(OH)3+3H+====Al3++3H2O
[解析] NH3·H2O是弱电解质,不能用OH-表示,应写分子式,Al(OH)3难溶用化学式表示,HCO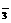 中的H难电离,不能写H+。
中的H难电离,不能写H+。
[答案] D
12.下列分解反应属于氧化还原反应的是
A.ZnCO3 ZnO+CO2
ZnO+CO2
B.5NH4NO3 4N2+2HNO3+9H2O
4N2+2HNO3+9H2O
C.Zn+CuSO4====ZnSO4+Cu
D.2Cu+O2 2CuO
2CuO
[解析] 只有ZnCO3、NH4NO3变化是分解反应,且NH4NO3中的N元素化合价发生变化。
[答案] B
11.下列各组离子在溶液中能够大量共存的是
A.Na+、SO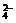 、K+、HCO
、K+、HCO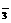 、H+
、H+
B.Na+、Cl-、HCO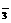 、NO
、NO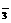 、OH-
、OH-
C.Na+、Mg2+、SO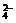 、Cl-、H+
、Cl-、H+
D.Na+、I-、MnO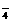 、H+、K+
、H+、K+
[解析] 离子反应可以从溶液呈现的环境来考虑,特别是酸、碱环境和氧化性环境。HCO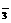 既不能与H+共存,又不能与OH-共存;而MnO
既不能与H+共存,又不能与OH-共存;而MnO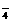 是一种强氧化性离子,I-具有较强的还原性。
是一种强氧化性离子,I-具有较强的还原性。
[答案] C
10.下列有关抗非典型肺炎的药品过氧乙酸的叙述肯定错误的是
A.该药品极难合成,目前无法大量生产
B.该药品具有较强的氧化性,可以用来杀菌消毒
C.该药品具有一定的稳定性,可能比过氧化氢稳定
D.该药品具有还原性,很不稳定
[解析] 从药品化学名称来看,该药品与过氧化氢等在结构上十分相似,但稳定性肯定比过氧化氢要强。
[答案] AD
9.下列反应一定不是离子反应的是
A.实验室用二氧化锰与氯酸钾共热制取氧气
B.工业上以石灰石煅烧制取生石灰
C.实验室用锌粒与稀硫酸制取氢气
D.实验室用石灰石(主要成分CaCO3)与稀盐酸制取二氧化碳气体
[解析] 离子反应一般都在水溶液中进行,且都有电解质参加反应。
[答案] AB
8.为了除去粗盐中Ca2+、Mg2+、SO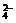 及泥沙,将粗盐溶于水,然后进行下列操作:①过滤②加足量的NaOH溶液③加足量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液,合理的操作顺序是
及泥沙,将粗盐溶于水,然后进行下列操作:①过滤②加足量的NaOH溶液③加足量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液,合理的操作顺序是
A.④⑤②①③ B.②⑤④①③
C.⑤②④①③ D.①④②⑤③
[解析] SO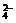 可使用Ba2+除去,Mg2+可用OH-除去;过量的Ba2+和原溶液中的Ca2+通过CO
可使用Ba2+除去,Mg2+可用OH-除去;过量的Ba2+和原溶液中的Ca2+通过CO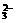 除去;过量的CO
除去;过量的CO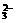 由H+除去,多余的盐酸通过加热蒸干而除去。
由H+除去,多余的盐酸通过加热蒸干而除去。
[答案] BC
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com