
题目列表(包括答案和解析)
4.设NA为阿伏加德罗常数的值,下列说法正确的是-------------------------------( )
A 2.3g金属钠变为钠离子失电子数为0.1NA B 18g水所含的原子数目为NA
C 在常温下22.4L氢气所含的原子数目为NA D 32g氧气所含的原子数目为NA
3.50mL0.5mol/L的硫酸铁溶液与25mL1.0mol/L的氯化铁溶液混合,若混合后体积不变,溶液中铁离子浓度约为------------------------------------------------------------( )
A 0.5mol/L B 0.67 mol/L C 0.75 mol/L D 1.0 mol/L
2.将0.1molNa投入足量水中,水共获得的电子个数为-----------------------------------( )
A NA/2mol B 2.3NAmol C 0.1NAmol D NAmol
1.在相同的温度下,下列气体密度最小的是---------------------------------------------( )
A CO2 B H2 C O2 D Cl2
23、A、B、C、D四种可溶性盐,它们的阳离子可能是 中的某一种,阴离子可能是
中的某一种,阴离子可能是 中的某一种。
中的某一种。
(1)若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
(2)若向(1)的四支试管中分别加盐酸,B盐溶液有沉淀生成,D盐溶液有无色无味气体逸出。 根据(1)、(2)实验事实可推断它们的化学式为:
A________,B________,C________,D________。
21、某溶液中含有Ag+、Ba2+、Mg2+离子,现用CO32-、Cl-、OH- 将这三种离子逐个进行沉淀分离,加入下列离子的先后顺序应当是:
。 22、向 溶液中逐滴加入
溶液中逐滴加入 溶液至中性,请写出发生反应的离子方程式_________________________________________。在以上溶液中继续滴加
溶液至中性,请写出发生反应的离子方程式_________________________________________。在以上溶液中继续滴加 溶液,请写出此步反应的离子方程式_________________________
_____。
溶液,请写出此步反应的离子方程式_________________________
_____。
20、某同学从一种未知的无色溶液中检验出Ag+、Ba2+,同时溶液的酸性很强,她还准备继续检验溶液中是否含有Cu2+、Cl-、CO32-、S2-、K+、Al3+、SO42-、SO32-、NO3-等离子。很显然,有些离子还必须检验,你认为必须检验的离子是 ;不必检验的离子,请简述理由 。
19、现有一包固体粉末,其中可能含有CaCO3、Na2CO3、Na2SO4、NaCl、CuSO4。进行如下实验:(1)溶于水得无色溶液;(2)向溶液中加 溶液生成白色沉淀,再加盐酸时沉淀消失。据上述实验现象推断 (1)一定不存在的物质是____________________。
溶液生成白色沉淀,再加盐酸时沉淀消失。据上述实验现象推断 (1)一定不存在的物质是____________________。
(2)一定存在的物质是______________。(3)可能存在的物质是__________________。
(4)对于可能存在的物质应如何进一步检验?写出简要的步骤和有关的离子方程式_________________________________________________________________________。
18、若金属阳离子An+1.2mol/L 10mL溶液恰好把0.4mol/L Na2CO3溶液30mL中的CO32-全部沉淀,则n等于( )
A.4 B.3 C.2 D.1
17、 某溶液加碱有沉淀析出,加酸有气体放出,该溶液中能共存的离子组是( )
A.  B.
B. 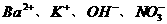
C.  D.
D. 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com