
题目列表(包括答案和解析)
2.目前,我国许多城市和地区定期公布空气质量报告,在空气质量报告中一般不涉及:
A.SO2 B.CO2 C.NO2 D.可吸入颗粒物
1.据最新报道,钬的放射性同位素16667Ho可有效地治疗肝癌。该同位素原子核内的中子数与核外电子数之差是:
A.32 B.67 C.99 D.166
26.用黄铁矿可以制取硫酸,再用硫酸制取化肥硫酸铵。[2NH3+H2SO4=(NH4)2SO4],燃烧
含FeS2 80%的黄铁矿75 t,生产出79.2 t 硫酸铵。若在制取硫酸铵时硫酸的利用率为
90%,则用黄铁矿制取硫酸时的损失率为多少?
25.在一定温度下,有530g Na2CO3溶液,其质量分数为25%,向该溶液中通入过量的CO2气体,完全反应后,经测定共析出不含结晶水的盐180g。试求在该温度下,析出盐的溶解度。
24.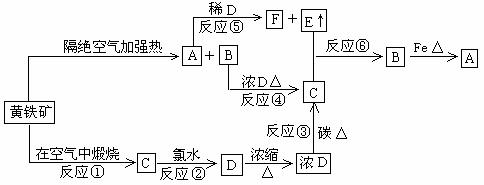 下图表示由黄铁矿为开始反应物的一系列变化,其中不含硫的反应产物已略去。
下图表示由黄铁矿为开始反应物的一系列变化,其中不含硫的反应产物已略去。
(1)写出化学式:A _______ B_________ C__________ D________ E_________
(2)写出化学方程式: ①_________________ ③_________________
④_________________ ⑥_________________
(3)写出离子方程式: ②_________________ ⑤_________________
23.过氧化氢(H2O2)俗名双氧水,医疗上可作外科消毒剂。
(1)向含有酚酞的NaOH溶液中滴加双氧水,溶液由红色褪至无色,主要原因是双氧水
具有___________性。
(2)将双氧水加入经酸化的高锰酸钾溶液中,溶液的紫红色消褪了,此时双氧水表现出
______性。
(3)久置的油画,白色部位(PbSO4)常会变黑(PbS),用双氧水“清洗”后又恢复原貌,
有关反应的化学方程式为_______________________________。
(4)如果将9.60×10-4mol AO4- 在溶液中还原成较低价态,需用0.100mol/L双氧水溶
液24.0mL,试通过计算确定A元素的最终价态为_________。
22.a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构
特点如下:
|
微粒代码 |
a |
b |
c |
d |
e |
f |
g |
|
原子核个数 |
单核 |
单核 |
单核 |
多核 |
双核 |
多核 |
多核 |
|
带电荷数 (单位电荷) |
0 |
1+ |
2+ |
0 |
1- |
1+ |
0 |
其中b的离子半径大于c的离子半径;d是由极性键构成的四原子极性分子;e与f可形成两个共价型g分子。试写出:
(1)a微粒的原子结构示意图__________________;
(2)b与c相应元素的最高价氧化物对应水化物的碱性强弱比较为_______>______(用
化学式表示);
高一化学 第4页共5页
(3)d微粒的电子式 ① ,它的结构呈 ② 形;
(4)e微粒是 ① ,f微粒是 ② (用化学式表示);
(5)g微粒所构成的晶体类型属_________晶体。
21.周期表前20号元素中,某两种元素的原子序数相差3,周期数相差1,它们形成化合
物时原子数之比为1:2。写出这些化合物的化学式_______________________。
20.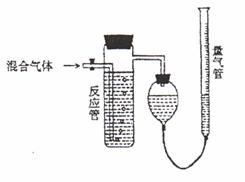 工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图。反应管中装有碘的淀粉
工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图。反应管中装有碘的淀粉
溶液。SO2和I2发生反应(N2、O2不与I2反应):
(1)混合气体进入反应管后,量气管内增加的
水的体积等于_________的体积(填写气体
的分子式)
(2)反应管内溶液蓝色消失后,没有及时停止
通气,测得的SO2含量_______(选填:偏
高,偏低,不受影响)
(3)反应管内的碘的淀粉溶液也可以用
_____________代替(填写物质名称)。
(4)若碘溶液体积为Va mL,浓度为C mol·L-1。
N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用C、Va、Vb表示SO2的体积百分含量为:______________________________________________________
19.要配制浓度约为2mol·L-1NaOH溶液100mL,下面的操作正确的是_____(填代号)
A 称取8g NaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加
入烧杯中,同时不断搅拌至固体溶解
B 称取8 g NaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体
完全溶解后用蒸馏水稀释至100mL
C 称取8 g NaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固
体溶解,再加水到刻度,盖好瓶塞,反复摇匀
D 用100mL量筒量取40mL 5mol·L-1 NaOH溶液,倒入250mL烧杯中,再用同一
量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com