
题目列表(包括答案和解析)
7、Zn+H2SO4=ZnSO4+H2↑
2KClO3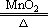 2KCl+3O2↑H2和O2都可用排水法收集。
2KCl+3O2↑H2和O2都可用排水法收集。
5、稳定性:H2S<NH3≈HCl 金属性:Na>Ca>Mg 原子半径:Al>S>Cl
22、(9分)把13g含有SiO2的CaCO3固体在高温下加热到质量不再减少为止,冷却后称重为8.6g。回答下列问题:
(1)生成的CO2在标准状况下的体积为_________L。
(2)求原物质中含SiO2的质量。
(3)试通过计算确定混合物发生的化学反应并写出发生反应的化学反应方程式。
答案:第一卷、1---5 BCCDB 6---10 DABAA 11---16 BAADDA
提示:
21、(6分)为了有效控制酸雨,我国政府已批准了《酸雨控制区和二氧化硫污染控制区方案》等法规。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
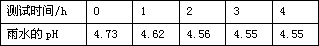
分析数据,回答雨水样品的pH变化的原因是(用化学方程式表示)
_________________________________________________________。
(2)研究结果表示:高烟囱可以有效地降低地表面SO2浓度。在20世纪的60年代-70年代的10年间,由发电厂排出的SO2增加了35%,但由于建筑高烟囱的结果,地面浓度降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?简述其理由。
(3)你认为减少酸雨产生的途径可采用的措施是________________。
①少用煤作燃料; ②把工厂烟囱造高;
③燃料脱硫; ④在已酸化的土壤中加石灰; ⑤开发新能源
A.①②③B.②③④⑤
C.①③⑤D.①③④⑤
20、(7分)为了验证氢气在空气中点燃发生化学反应生成物除水以外,还有过氧化氢。某学生设计了如下两个对比实验:
(1)在点燃的氢气火焰上方用湿润的淀粉碘化钾试纸检验,发现淀粉碘化钾试纸变蓝;
(2)在点燃的酒精灯火焰上方用湿润的淀粉碘化钾试纸检验,发现淀粉碘化钾试纸不变蓝(已知酒精的分子式为C2H5OH);
通过以上两个对比实验请回答下列问题:
(1)试写出以上两个燃烧的主要化学反应的化学方程式:
_______________________________________________________;
_______________________________________________________。
(2)试说明上述实验能证明氢气在空气中燃烧的生成物中含有氧化氢的理由_______________________________;写出氢气与空气中氧气发生反应生成过氧化氢的化学方程式及过氧化氢使湿润的淀粉碘化钾变蓝的离子反应方程式:
_______________________________________________________;
_______________________________________________________。
19、(9分)A、B、C是三种短周期元素的单质,甲、乙是两种常见的化合物,这些单质、化合物之间存在如下图所示关系,反应条均件未注明,回答下列问题:
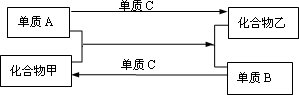
下列(1)-(3)中的A不在同一主族。
(1)若A为ⅢA族元素,则A是__________,B为________,C为______。
(2)若化合物甲在常温、常压下为液态,则组成化合物甲的元素所属类别为_________(填金属或非金属),单质A与化合物甲反应的化学方程式为: ________________。
(3)若化合物乙为氧化物,则化合物甲所属物质类别为___________(填配、碱、盐、氧化物、氢化物),单质A与化合物甲反应的化学方程式为:____________________。
18、(12分)I为了比较硫与碳的非金属性的强弱,某同学想通过比较两种元素的最高价氧化物对应的水化物的酸性强弱来验证硫与碳的非金属性的强弱,采用了下图中的甲、乙装置:
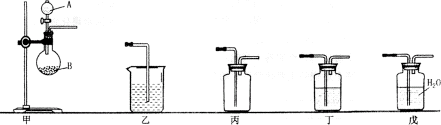
(1)仪器A中应盛放的药品是___________,仪器B中应盛放的药品是________,装置乙中应盛放的药品是___________。
(2)B中发生反应的离子方程式为:______________________________;
在装置乙中观察到的现象是:_______________________________。
(3)该实验能证明硫与碳非金属性强弱的理论依据是:________________________________________。
Ⅱ实验室用MnO2和浓盐酸反应制取氯气,如果使用上述甲、乙、丙、戊五种装置,请回答下列问题:
(4)上述装置图中还缺少的实验用品是_______________________。
(5)配备实验用品后,进行实验,B中发生反应的离子方程式为:_______。
(6)若要制得纯净的氯气,上述装置的连接顺序是(用甲、乙、丙、丁、戊表示连接的先后顺序)__________________,装置丁中盛放的试剂是________________。
17、(9分)通过实验证明KClO3的成分里含有钾、氧和氯三种元素,完全下列实验报告。

16、将一定量的锌与100mL 18.5mol/L浓H2SO4充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况下),将反应后的溶液释释至1L,测得溶液的c(H+)=0.1mol/L,则下列叙述中错误的是( )
A.气体A中SO2和H2的体积比为4:1
B.反应中共转移电子为3mol
C.反应中共消耗锌97.5g
D.气体A为SO2和H2的混合物
第Ⅱ卷(非选择题共52分)
本卷共6道题
15、为方便某些化学计算,有人将98%浓硫酸表示成下列形式,其中合理的是( )
①H2SO4·1/9H2O ②H2SO4·H2O
③H2SO4·SO3 ④SO3·10/9H2O
A.② B.③④
C.②④ D.①④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com