
题目列表(包括答案和解析)
7. 目前含有元素硒(Se)的保健品已开始涌入市场,已知它与氧同主族,而与钙同周期,下列关于硒的有关描述中不正确的是 ( )
A.原子序数24 B.最高价氧化物为SeO3,为酸性氧化物
C.原子半径比钙小 D.气态氢化物化学式为H2Se,性质不稳定
6. 下列物质中既有离子键又有共价键的是( )
A.CaCl2 B.H2O2 C.KOH D.H2S
5. 元素X的原子获得3个电子或元素Y的原子失去2个电子后,它们的电子层结构与氖原子的电子层结构相同,X、Y两种元素的单质在高温下得到的化合物的正确的化学式为( )
A. Y3X2 B. X2 Y3 C. X2Y3 D. Y2X3
4. 原子序数在20号以前的元素,原子最外层电子数等于次外层电子数的有( )
A.1种 B.2种 C.3种 D.4种
3. 元素性质呈周期性变化的决定因素是( )
A.元素原子半径大小呈周期性变化 B.元素原子量依次递增
C.元素原子最外层电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化
2. 据报载我国最近合成多种元素的新的同位素,其中一种是18572Hf(铪),它的中子数是( )
A.72 B.113 C.185 D.257
1. 19世纪中叶,门捷列夫的突出贡献是( )
A.提出原子学说 B.发现元素周期律 C.提出分子学说 D.最早发现了氧气
35.某元素的同位素ZAX,它的氯化物XCl21.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)把X的单质放入水中,有何现象?写出反应的化学方程式。
34.有A、B、C三种元素,已知5.75gA单质跟盐酸完全反应,在标准状况下可产生2.8L氢气和0.25molACln;B的气态氢化物的分子式为H2B,其相对分子质量与B的最高价氧化物的水化物相对分子质量之比为1∶2.88,B核内质子数与中子数相等;C和B可以形成CB2型液态化合物,并能溶解B的单质,试回答下列问题:
(1)试通过计算推断A、B、C各是什么元素?
(2)写出A、B的离子结构示意图、B在周期表中的位置、CB2的化学式;
(3)用电子式表示Ca和B形成化合物的过程。
33.(4分)某离子晶体晶胞结构如下图所示,X位于立方体的顶点,Y位于立体中心。试分析:
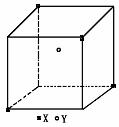
(1)体中每个Y同时吸引着______________个X,每个X同时吸引着______________个Y,该晶体化学式为______________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有______________个。
(3)晶体中距离最近的2个X与1个Y形成的夹角∠XYX的度数为______________(填角的度角)。
(4)设该晶体的摩尔质量为Mg·mol-1,晶体密度为ρg·cm-3,阿伏加德罗常数为Na,则晶体中两个距离最近的X中心间的距离为______________cm。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com