
题目列表(包括答案和解析)
22.有五瓶溶液分别是:①10mL0.60mol/LNaOH水溶液,②20mL0.50mol/LH2SO4水溶液,③30mL0.40mol/LHCl水溶液,④40mL0.30mol/HAc水溶,⑤50mL0.20mol/L蔗糖水溶液,以上各瓶溶液所含离子、分子总数的大小顺序是
A.①>②>③>④>⑤ B.②>①>③>④>⑤
C.②>③>④>①>⑤ D.⑤>④>③>②>①
第Ⅱ卷(78分)
选择题答题表
21.由钾和氧组成的某种离子晶体含钾的质量分数是78/126,其阴离子只有过氧离子(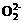 )和超氧离子(
)和超氧离子(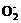 )两种。在此晶体中,过氧离子和超氧离子的物质的量之比为
)两种。在此晶体中,过氧离子和超氧离子的物质的量之比为
A.2:1 B.1:1 C.1:2 D. 1:3
20.若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1氨水的质量分数,且知 2a=b,则下列推断正确的是(氨水的密度比纯水的小)
A 2ω1=ω2 B 2ω2=ω1 C ω2>2ω1 D ω1<ω2<2ω1
19.质量分数为a的某物质的溶液mg与质量分数为b的该物质的溶液ng混合后,蒸发掉pg水,得到的溶液每毫升质量为qg,物质的量浓度为c。则溶质的分子量(相对分子质量)为
A.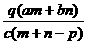 B.
B.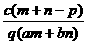
C.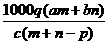 D.
D.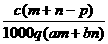
18. 依照阿伏加德罗定律,下列叙述中正确的是
A.同温同压下两种气体的体积之比等于摩尔质量之比
B.同温同压下两种气体的物质的量之比等于密度之比
C.同温同压下两种气体的摩尔质量之比等于密度之比
D.同温同体积下两种气体的物质的量之比等于压强之比
17.在一定条件下,RO3n-和氟气可发生如下反应
RO3n-+F2+2OH- RO4-+2F-+H2O
从而可知在RO3n-中,元素R的化合价是
A.+4 B.+5 C.+6 D.+7
16.下列溶液中c(Cl-)与50ml 1 mol/L氯化铝溶液中的c(Cl-)相等的是
A.150mL 1 mol/L NaCl B.75mL 1.5 mol/LMgCl2
C.150mL 3 mol/L KCl D.25mL 2 mol/L AlCl3
15.VLFe2(SO4)3溶液中,含Fe3+离子mg,则溶液中SO42-离子的物质的量浓度为
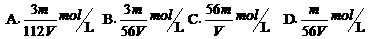
14. 同温同压下, 等质量的二氧化硫和二氧化碳相比较, 下列叙述正确的是
A.密度比为16:11 B.密度比为11:16
C.体积比为1:1 D.体积比为11:16
13. 浓度为0.50mol·L-1的某金属阳离子Mn+的溶液10.00mL,与0.40mol·L-1的NaOH溶液12.50mL完全反应,生成沉淀,则n等于
A. 1 B. 2 C. 3 D. 4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com