
题目列表(包括答案和解析)
1. 二十世纪九十年代初,国际上提出了“预防污染”这一概念。能造成大气污染的主要物质是( )
A.二氧化碳、氮气、氯气、烟雾
B.水蒸气、氯化氢、氨气、烟尘
C.二氧化硫、氮氧化物、一氧化碳、烟尘
D.氯化氢、二氧化硫、粉尘、氢气
31.(6分)向300mLKOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下
蒸发溶液,得到白色固体。请回答下列问题:
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,
并分别列出。
(2)若通入CO2气体为2.24L(标准状况下),得到11.9g的白色固体。请通过计算确定
此白色固体是由哪些物质组成的?
高中学生学科素质训练
30.(4分)16.6g卤化钾与足量的硝酸银溶液反应,生成23.5g沉淀,求该卤化钾中卤原子
的相对原子质量。
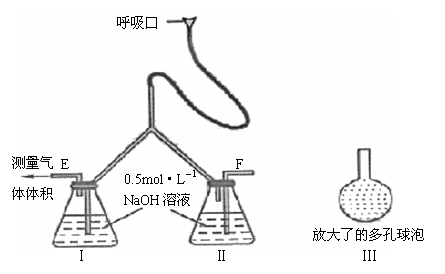
29.为了测定人体新陈代谢呼出气体中CO2的体积分数,某学生课外小组设计了如下图的实
验装置,实验中用过量NaOH溶液吸收气体中的CO2,准确测量瓶I中溶液吸收CO2后
的增重及剩余气体的体积(实验时只用嘴吸气和呼气),请填空:
(1)图中瓶II的作用是_____________________________________________________。
(2)对实验装置尚有如下A.B.C.D四种建议,你认为合理的是(填代号)______
A.在E处增加CaCl2干燥管 B.在F处增加CaCl2干燥管
C.在E和F两处增加CaCl2干燥管 D.不必增加干燥管
(3)将插入溶液的管子下端改成具有多孔的球泡(图中的III),有利于提高实验的准确
度,其理由是__________________________________________________
_______________________________________________________________________
_____________________________________________________________________。
(4)实验时先缓缓吸气,再缓缓呼气,反复若干次,得如下数据:瓶I溶液增重a g,收
集到的气体体积为b L(标准状况)。在呼出气体中CO2的体积分数是(列出算式):
______________________________________________________________________。
(5)实验中若猛吸猛呼,会造成不安全后果,猛吸时会_____________________________
________________________________________;猛呼时会_____________________
_____________________________________________________________________。
28. 有两种白色固体为AgCl和BaSO4,设计一个实验把它们区别开来。
有两种白色固体为AgCl和BaSO4,设计一个实验把它们区别开来。
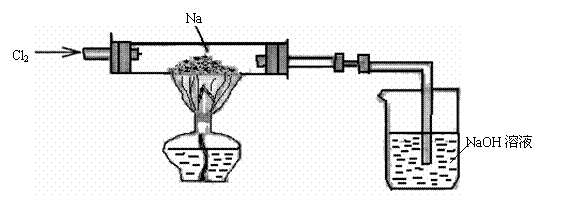
27.(6分)按下图装置好实验仪器和药品,通入Cl2,先排出装置中的空气,直至玻璃中充
满足够气体时,管内气体呈__________色,加热金属钠,使其熔化并开始剧烈反应,看
到的现象是钠燃烧的火焰呈__________(填颜色),并有________产生,反应完全后,
停止加热,冷却后,看到试管壁上有_________色固体附着,尾气吸收的离子方程式是
__________________________________________________,实验室制Cl2的化学方程式
是_______________________________________________________________________。
26.(4分)将50g16%的Na2CO3溶液和65.6g8%的Na2CO3溶液混合,得到密度为1g/cm3的
溶液。该溶液溶质的质量分数为____________;该溶液物质的量浓度为__________。
25.(4分)从海水中制取溴的过程是把Cl2通入加热到90℃, pH=3.5的卤水中,将Br-氧
化为Br2,用空气吹出生成的Br2,被Na2CO3溶液吸收得到NaBr和NaBrO3混合液 ,
再用酸酸化混合液,即可得到Br2。写出有关的离子方程式。
(1)Na2CO3溶液吸收Br2:_____________________________________________。
(2)用酸酸化混合液制取Br2:_________________________________________。
24.(3分)称取一定质量的纯碱,溶于水后跟盐酸完全反应放出CO2。用“增多”或“减少”
回答以下问题:
(1)若纯碱中含有NaHCO3,则所需盐酸用量____ _______。
(2)若纯碱中含K2CO3,则所需盐酸用量________ _______。
(3)若纯碱中含NaCl,则所需盐酸用量____ ____________。
23.(6分)在含有35.8克Na2CO3和NaHCO3溶液内,加入1摩/升的盐酸700毫升,反应完
全后可以生成8.96升CO2(标准状况)。问:(1)其中__________物质过剩;(2)溶液
中Na2CO3有__________g;(3)若上述溶液内加入1摩尔的盐酸450毫升,反应完全后,
在标准状况下可生成CO2__________升。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com