
题目列表(包括答案和解析)
26.6g/L
0.05 mol 0.1 mol
消耗盐酸0.1+0.1=0.2(mol)。故该盐酸物质的量浓度为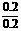 =1(mol/L)。
=1(mol/L)。
0.05 mol 0.1 mol
Ca(HCO3)2+ 2HCl = CaCl2+2CO2↑+2H2O
0.05 mol 0.05 mol 0.05 mol 得沉淀0.05×100=5(g)。
CaCO3+ 2HCl = CaCl2+CO2↑ +H2O
Ca(OH)2+CO2=CaCO3↓+H2O
0.1 mol 0.1 mol 0.1 mol
CaCO3+ CO2 +H2O = Ca(HCO3)2
23.(1)SiCl4 SiO2 (2)由粗硅制取高纯度的精硅 (3) SiO2+2NaOH=Na2SiO3+H2O
|
(2)C+ CO2===2CO CO2+NaOH=NaHCO3 NaHCO3+NaOH=Na2CO3+H2O
21.(1)以防止试管Ⅲ内的Na2O2和外界相通时发生吸潮现象 (2)浓H2SO4 Na2O2和干燥的CO2不反应 (3)带火星的小木条在试管Ⅱ的液面上剧烈燃烧,同时Ⅲ内Na2O2淡黄色变为白色 (4)2 Na2O2+2 C18O2+2H218O=2Na218O3+ O2↑+2H2O
|
GeO2+2H2====Ge+2H2O
+2H2O ③加盐酸,过滤 CaO+2HCl=CaCl2+H2O ④加CS2溶液,过滤、无 ⑤加盐酸,过滤 Fe2O3+6HCl=2FeCl3+3H2O
20.澄清石灰水 NaOH溶液 灼热的CuO;灼热的铜网 高温煅烧
26.(7分)检验某病人血液中的含钙量,取10mL血液,稀释后用(NH4)2SO4溶液处理,生成CaC2O4沉 淀,过滤沉淀将其溶于强酸中,然后用0.5 mol,/L KMnO4溶液滴定,用去高锰酸钾溶液1.20mL。有关反应如下:
Ca2++C2O42-=CaC2O4↓
CaC2O4+H2SO4=CaSO4+ H2C2O4
2 H2SO4 + H2C2O4+2KMnO4
=K2SO4+2MnSO4+10CO2↑+8H2O计算病人血液中的含钙量(g/L)。
第七章 硅和硅酸盐
段段清--单元综合测试
25.(6分)向含0.1 mol Ca(OH)2的石灰水中通入3.36 L(标准状况)CO2,充分反应后,能产生多少克沉淀?要使沉淀及所在的混合溶液与200mL盐酸恰好反应至中性溶液,则该盐酸的物质的量浓度是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com