
题目列表(包括答案和解析)
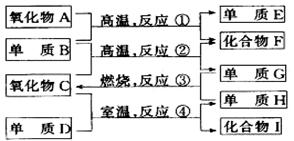
25、(8′)有物质A-I,它们之间的相互转化关系如下图所示。
已知:①单质E可用为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈弱酸性,它能与氧化物A发生非氧化还原反应生成C和另一种化合物。
据此,请回答:
⑴化合物F是 。
⑵化合物I是_ 。
⑶反应②的化学方程式是_____ ___ 。
反应④的化学方程式是________ 。
24、(6′)甲、乙、丙三位同学各设计了一个实验,并都认为,如果观察到的现象和自己设计的方案一致,即可确证试液中含有SO42-。
甲的实验方案是:试样A(无色溶液) 白色沉淀
白色沉淀 沉淀不溶解;
沉淀不溶解;
⑴乙认为甲的实验不严谨,因为试样A中若含有 离子(仅填一种),也会有此现象。
乙的实验方案是:试样B(无色溶液) 白色沉淀
白色沉淀 沉淀不溶解;
沉淀不溶解;
⑵丙认为乙的实验不严谨,因为试样B中若含有 离子(仅填一种),也会有此现象。
丙的实验方案是:试样C(无色溶液) 现象Ⅰ
现象Ⅰ 现象Ⅱ;
现象Ⅱ;
⑶若丙方案合理,则回答:其中试剂I是 ,现象I是 ;试剂II是 ,现象II是 。
 (你若认为丙方案不合理,以上四空可以不填)
(你若认为丙方案不合理,以上四空可以不填)
23、(7′)⑴工业上制取漂白粉的化学方程式为 。
⑵漂白粉的有效成分是 ,向其溶液中通入少量CO2,反应的化学方程式是
。
⑶若向漂白粉有效成分的溶液中通入适量SO2,有学生认为反应的离子方程式为:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO。你认为是否合理,简述原因:
。
22、(10′)有原子序数均小于20的A、B、C、D四种元素,已知:①A和B在同一主族,C和D在同一周期;②四元素相互间可形成A2C、A2C2、B2C2、DC2等化合物;③B的阳离子与C的阴离子核外电子层结构相同;④B2C2与A2C或DC2反应都生成C2气体;⑤B的单质与A2C反应生成A2气体,A2与C2混合遇火可发生爆炸,生成常温下无色无味的液体A2C。试回答:
⑴写出A和D两元素的名称:A 、D ;画出B离子和C离子的结构示意图:
B 、C ,两种离子中,半径较小的是 (写离子符号)。
⑵写出A2C2、B2C2、DC2的电子式:
A2C2 ;B2C2 ;DC2 。
⑶写出B2C2与DC2反应的化学方程式 。
21、(5′)A、B两种气体都是大气污染物,严格禁止向大气中排放,在工业上常用碱液来吸收。已知A具有还原性,B是一种单质,其水溶液都具有漂白作用。
⑴A是 ,B是 。
⑵若A、B同时作用于一潮湿的有色布条上,其漂白效果会 (填增强、减弱或不变),原因是(用化学方程式表示) 。
20、已知反应:KClO3+6HCl=KCl+3Cl2↑+3H2O,若用K35ClO3与H37Cl作用,下列说法正确的是
A、此反应中,每生成3molCl2转移电子6mol
B、生成物KCl中只含有37Cl
C、生成的Cl2中只含有35Cl
D、生成Cl2的相对分子质量为72
19、下列各组离子,能在溶液中大量共存的是
A、Ag+、K+、I-、NO3- B、H+、Na+、CO32-、MnO4-
C、Ba2+、Al3+、Cl-、SO42- D、H+、Mg2+、Cl-、 SO42-
18、24mL浓度为0.05mol/L的Na2SO3溶液,恰好与20mL浓度为0.02mol/L的K2Cr2O7溶液完全反应,则Cr元素在还原产物中的化合价为
A、+4 B、+3 C、+2 D、+1
17、二硫化碳(液体)能够在氧气中完全燃烧,生成二氧化碳和二氧化硫。若在标准况状下,用0.1 mol二硫化碳在1mol氧气中完全燃烧,则反应后气体混合物在标准况状时的体积为
A、22.4L B、6.72L C、13.44L D、15.68L
16、下列变化中,不需要破坏化学键的是
A、食盐熔化 B、干冰气化
C、氯化氢溶于水 D、氯化铵受热分解为氨气和氯化氢
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com