
题目列表(包括答案和解析)
|
微粒种类 |
原子核 |
电子 |
|
|
质子 |
中子 |
||
|
(1)电性和电量 |
每个质子带1个单位正电荷 |
不显电性 |
每个电子带1个单位负电荷 |
|
(2)相对质量 |
1.007 |
1.008 |
1/1836 |
|
(3)作用 |
质子数决定元素种类 |
中子数与质子数决定原子种类 |
核外电子数与核内质子数决定元素性质 |
|
(4)数量关系 |
①在原子中:核电荷数=核内质子数=核外电子数 ②在阳离子中:核内质子数-核外电子数=所带电荷数 ③在阴离子中:核外电子数-核内质于数:所带电荷数 ④质子数+中子数=质量数;核素的近似相对原子质量 |
2.同位素的性质
① 同位素的性质化学几乎完全相同,是由于原子核外电于排布相同;物理性质不同,由于它们的中子数不同。
② 在天然存在的某种元素里,不论是游离态还是化合态,各种同位素所占的原子百分比一般不变。
1.概念比较
(1)元素是具有相同核电荷数(质子数)的同一类原子的总称;核素是具有一定数目的质子和一定数目的中子的一种原子;同一元素不同核素之间互称为同位素。
(2)标号为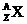 的核素,其质子数为Z,中子数为A-Z,质量数为A。
的核素,其质子数为Z,中子数为A-Z,质量数为A。
[知识结构]
22.X、Y、Z都属于短周期元素,已知它们的原子序数Y<Z<X.又知Z原子M层的电子数与K层电子数相等,X原子最外层电子数是Z原子最外层电子数的2倍,而Y原子最外层电子数则是Z原子最外层电子数的3倍.三种元素之间可分别形成化合物ZY、XY2、及Z2X等.据此可知:
(1)X是________,Y是________,Z是________
(2)写出高温ZY与XY2之间反应的化学方程式:________,二者可以发生反应的原因是________.
(3)Z与X的单质隔绝空气加热可得化合物Z2X,Z2X与盐酸反应可制得X的气态氢化物.分别写出生成Z2X以及Z2X与盐酸反应的化学方程式________.
21.A、B、C、D、E、F为原子序数依次增大的主族元素.已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,且均生成盐和水.D元素原子的最外层电子数比次外层电子数少4.E元素原子的次外层电子数比最外层电子数多3,试回答:(1)写出下列元素的符号:A________、D________、E________.(2)用电子式表示B、F形成化合物的过程________.(3)A、C两种元素最高价氧化物对应的水化物相互反应的离子方程式为________.
20.Li3N是离子晶体,它与水作用可生成NH3,试回答
(1)写出Li3N的电子式________
(2)写出Li3N与水反应的化学方程式________
(3)微粒半径关系,Li+________N3-,Li________N(填>、<、=)
19.已知A、B、C、D四种元素的原子中质子数都小于18,它们的核电荷数A<B<C<D,A与B可生成化合物AB2,每个AB2分子中含有22个电子,C元素原子的次外层电子数为最外层电子数的2倍,D元素原子的最外层电子数比次外层少一个,则A、B、C、D四种元素的名称分别为________、________、________、________.
18.X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物时,其化学式为________;若XY2为共价化合物时,其化学式为________.
17.分别由氕、氘、氚组成的单质(S、T、P)都是1g,其中它们的原子个数之比为________,电子数之比为________,密度之比为________,体积之比为________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com