
题目列表(包括答案和解析)
9.将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能
有 ( )
A.Cu、Fe3+ B.Fe2+、Fe3+ C.Cu、Cu2+、Fe D.Cu、Fe2+、Fe
8.金属钠和水(含几滴酚酞)的反应是一个重要的实验,能从该实验获得的信息中说
明金属钠具有的性质是:① 密度较小 ②熔点较低 ③ 硬度较小 ( )
④还原性强 ⑤ 该反应生成相应的碱 ⑥ 该反应是放热反应
A.①②③④⑤ B.①②④⑤⑥ C.除③⑥之外 D.全部
7.用铝箔包着2.3g金属钠,放入50ml水中,放出的H2体积(标准状况)是
A.等于2.24L B.等于1.12L C.大于1.12L D.小于1.12L
6.硫酸亚铁溶液中含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入
下列哪种物质 ( )
A.锌粉 B.铁粉 C.镁粉 D. 铝粉
5.下列反应的离子方程式书写正确的是 ( )
A.钠和冷水反应: Na+2H2O=Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液: Al+2OH-=AlO2-+H2
C.铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2
D.铜和硝酸银溶液反应: Cu + 2Ag+ = 2Ag + Cu2+
4.下面有关Na2CO3 与NaHCO3的叙述错误的是 ( )
A.相同浓度溶液的碱性:Na2CO3比NaHCO3强
B.在水中的溶解度:Na2CO3比NaHCO3大
C.与同浓度的硫酸反应时,Na2CO3比NaHCO3剧烈
D.NaHCO3能与NaOH反应,而Na2CO3不能
3.铝在人体中积累可使人慢性中毒,世界卫生组织将铝确定为食品污染源之一而加以控制。铝在下列使用场合中,必须加以控制的是 ( )A.制铝合金门窗 B.制牙膏皮 C.制防锈油漆 D.炼铝厂制造铝锭
2.少量的金属钠长期暴露在空气中,它的最终产物是
A.NaOH B.Na2CO3•10H2O C.Na2CO3 D.NaHCO3
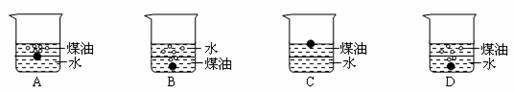
1.向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中轻缓地加入绿豆大
小的金属钠,可能观察到的现象是 ( )
22.在盛有一定量浓硝酸的试管中加入6.40g铜片发生反应。请回答:
(1)开始阶段,观察到实验现象为
反应的化学方程式是 。
(2)反应结束后,铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式是 。
(3)若6.40g铜片消耗完时,共产生气体2.80L(标准状况)。求整个反应过程中所消耗
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com