
题目列表(包括答案和解析)
3.下列物质露置在空气中质量会减少的是
A.Na2O固体 B.浓H2SO4 C.NaCl晶体 D.浓HCl
2.酸雨的形成主要是由于
A.森林遭到乱砍滥伐,破坏了生态平衡 B.工业上大量燃烧含硫燃料
C.金属矿石的冶炼 D.大气中二氧化碳含量增多
1.下列燃料中,不属于化石燃料的是
A.汽油 B.煤 C.天然气 D.氢气
25. 我国推广食用加碘盐。根据GB5461--《国家食用盐标准》,碘元素含量为20-50mg/kg为合格。质量监督部门为检测某品牌加碘盐是否合格,进行了如下实验:称取250g 某品牌加碘盐样品,在酸性条件下用足量KI溶液将其中IO3-全部转化成I2,生成的I2再用0.010mol/L的硫代硫酸钠溶液滴定,滴定到终点时用去24 mL。
有关反应如下:(未配平)
①IO3-+I-+H+-I2+H2O
②I2+S2O32--I-+S4O62-
⑴写出配平了的上述两个反应方程式 、 ;
⑵用硫代硫酸钠溶液滴定I2时,应用_________作指示剂,滴定到终点的现象是________;
⑶试通过计算说明该加碘食盐是否为合格产品(写出具体的计算过程)。
高二化学(综 合 题)检测题
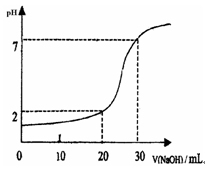
24. 右图为10mL一定物质的量的盐酸用一定浓度的NaOH溶液中和的图示,依据图示推算出HCl和NaOH的物质的量浓度各是多少?(注:溶液混合时造成的体积缩小忽略不计)
23. 实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。
(1)根据什么现象可判断铜跟浓硫酸反应有SO2生成______________________。
根据什么现象可判断铜跟浓硫酸反应有硫酸铜生成________________________。
写出甲装置中发生的主要反应的化学方程式_____________________________。
(2)你在实验室中进行这个实验时,除了1.小题中指到的实验现象外,还可以观察到许多其它的实验现象,请写出两种:____________________________________、___________________________________。
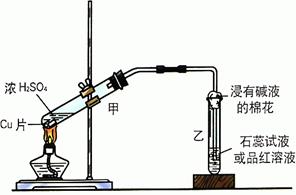 (3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,写出棉花中发生反应的化学方程式___________________________________。
(3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,写出棉花中发生反应的化学方程式___________________________________。
22. 常温下,取两片质量相等、外形和组成相同表面经过砂纸打磨(完全除掉了氧化物)的铝片,分别加入到盛有体积相同、c(H+)相同的稀硫酸和稀盐酸溶液的两支试管(相同体积)中,铝片在稀盐酸中产生的氢气的速率比在稀硫酸中快。
(1)写出以上反应的离子方程式_____________________________________________;
(2)你认为出现以上现象的可能原因是:
假设①___________________________________________________________;
假设②___________________________________________________________________。
(3)请设计实验对以上的假设进行验证:
①_____________________________________________________________________
___________________________________________________________________________;
②__________________________________________________________________________
_____________________________________________________________________________。
(4)如果上述假设都成立,要使以上稀硫酸与铝反应产生的氢气速率加快,可以采取的措施有:
①______________________________________________________________________;
②______________________________________________________________________;
③______________________________________________________________________;
④______________________________________________________________________。
21. 下图为某些常见物质之间的转化关系。已知:A、B、I中含有相同的阳离子且都是XY2型化合物,I是常用的干燥剂,单质F常用作自来水消毒。
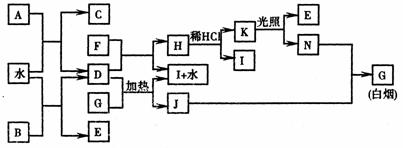
请按要求填空:
(1) A的电子式是 、B的电子式是 、
K的结构式是 、C的结构式是 ;
(2) D与G反应的化学方程式是 ;
(3 含1mol N的稀溶液与足量稀氢氧化钠溶液完全中和,放出57.3kJ的热量,则表示该反应中和热的热化学方程式为: 。
20. 从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物。
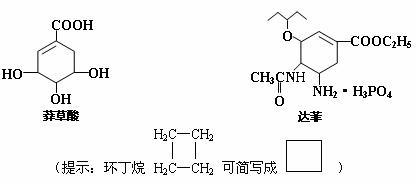
(1)莽草酸中含有的官能团有 ;(写名称)
(2)根据达菲分子的结构推测它可能发生的反应类型有: ;
(3)请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):
____________________________________________;
19. 在一定条件下,在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)

⑴若起始时两边分别投入2 mol SO2、1 mol O2;1 mol N2、3 mol H2,达到平衡后,隔板能否处于中央 (填“是”或“否”)。
⑵若起始时投入2 mol SO2、1 mol O2;1 mol N2、2 mol H2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字);
⑶若起始时投入2 mol SO2、1 mol O2;1 mol N2、a mol H2、0.1 mol NH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于中央,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com