
题目列表(包括答案和解析)
3.
氧化还原反应中电子转移的表示方法
2. 氧化还原反应 实质:电子发生转移
判断依据:元素化合价发生变化
物质的分类(可按组成、状态、性能等来分类)
物质 混合物 非均匀混合物
均匀混合物
纯净物 单质 非金属单质
金属单质
化合物 有机化合物
无机化合物 氧化物 金属氧化物
非金属氧化物
…
酸
碱
盐
…
物质的转化(反应)类型
四种基本反应类型:化合反应,分解反应,置换反应,复分解反应
化学反应 本质 氧化还原反应 化学反应 离子反应
非氧化还原反应 非离子反应
氧化还原反应
1.氧化还原反应:有电子转移的反应
35(4分)某硫酸试剂瓶的标签上写着:密度为1.84g·cm-3,质量分数为98%。试计算:
⑴该硫酸溶液中硫酸的物质的量浓度是多少?
⑵要多少毫升这种浓硫酸才能配制100mL1.84mol·L-1硫酸溶液?
36(6分)用1L 1.0 mol·L-1 NaOH溶液吸收17.92L CO2(标准状况)后溶液体积不变。求所得溶液中的CO32-和HCO3-的物质的量浓度。
(已知可能的反应为:2NaOH+ CO2== Na2CO3+H2O,NaOH+ CO2==NaHCO3)
32(7分)喷泉是一种常见的自然现象,其产生原因是存在压强差。
⑴右上图为化学教学中用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
 A.HCl和H2O B.O2和H2O
C.NH3和H2O D.CO2和NaOH溶液
A.HCl和H2O B.O2和H2O
C.NH3和H2O D.CO2和NaOH溶液
⑵某学生积极思考产生喷泉的其他办法,并设计了如右下图所示的装置。
①在锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
②在右下图锥形瓶外有一水槽,瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是
A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
这种方法产生喷泉的原理是
③比较右上图和右下图两套装置,从产生喷泉的原理来分析,右上图是 上部烧瓶内气体压强;右下图是 下部锥形瓶内气体压强。
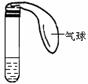 ⑶常见的人造喷泉及火山爆发的原理与上述 (填右上图或右下图)装置的原理相似。
⑶常见的人造喷泉及火山爆发的原理与上述 (填右上图或右下图)装置的原理相似。
33(4分)某学生课外活动小组利用右图所示装置分别做如下实验:
⑴在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是 溶液;加热时溶液由红色逐渐变浅的原因是: 。
⑵在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是
溶液;加热时溶液由无色变为红色的原因是: 。
34(3分)试简要回答下列问题
⑴焰色反应操作可简要地用五个字表示“洗、烧、醮、烧、洗”,第一个“烧”的作用是
;
⑵配制200mL0.1mol·L-1氯化钠溶液时必不可少的玻璃仪器是 ;
⑶酒精不能用于萃取碘水中的碘,其原因是 。
27(4分)
⑴电解食盐水的化学方程式:
⑵氯气通入氢氧化钠溶液中的离子方程式:
⑶氯化铁溶液中加入硫氰化钾的离子方程式:
28(8分)
⑴在化学方程式中标出下列反应的电子转移方向和数目,并回答问题。
3Cl2+6KOH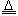 5KCl+KClO3+3H2O 被氧化的氯元素占全部氯元素总质量的 %;氧化剂和还原剂质量比为 ;氯气表现
性;当转移1mol电子时有 mol KClO3生成。
5KCl+KClO3+3H2O 被氧化的氯元素占全部氯元素总质量的 %;氧化剂和还原剂质量比为 ;氯气表现
性;当转移1mol电子时有 mol KClO3生成。
⑵写出指定物质的化学式:胆矾 ;孔雀石 ;明矾 。
29(4分)从Cl2分别与KBr、KI,Br2与KI的反应中,你发现的规律是(能归纳几条写几条):
。
30(2分)某无色溶液中可能有SO42-、OH-、CO32-、Cl-等阴离子中的一种或几种。
(1)若该溶液中还存在相当浓的H+,则溶液中可能含有的阴离子是 (多写要扣分)
(2)若该溶液中还存在较多量的Ba2+,则溶液中可能含有的阴离子是 (多写要扣分)
31(6分)a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: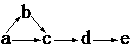
其中: a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物。
⑴如果a是一种淡黄色粉末固体,试推断这五种物质。用名称表示:
a ;c ;e 。
 ⑵如果a是一种常见气体,试推断这五种物质。用化学式表示:
⑵如果a是一种常见气体,试推断这五种物质。用化学式表示:
a ;c ;e 。
第Ⅱ卷 (共48分)
26.根据下列反应判断物质的氧化性由强到弱的顺序正确的是
①Cl2+2KI==I2+2KCl ②2FeCl3+2HI==I2+2FeCl2+2HCl
③2FeCl2+Cl2==2FeCl3 ④I2+SO2+2H2O==2HI+H2SO4
A.Cl2>I2>Fe3+>SO2 B.Fe3+>Cl2>I2>SO2
C.Cl2>Fe3+>SO2>I2 D.Cl2>Fe3+>I2>SO2
班 号 姓名 成绩
25. 将铜片投入到稀硫酸中,铜片不溶,再加入下列试剂后,仍不能使铜片溶解的是CD
A.新制漂白粉 B.硫酸钠晶体 C.硝酸钠晶体 D.氯化铁晶体
24. 制印刷电路时常用氯化铁作为腐蚀液。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,此时可能发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2、2FeCl3+Fe=3FeCl2、Fe+CuCl2=FeCl2+Cu,反应结束后,下列结果不可能出现的是
A. 烧杯中的单质有铜无铁 B. 烧杯中的单质有铁无铜
C. 烧杯中的单质铜、铁都有 D. 烧杯中的单质铜、铁都无
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com