
题目列表(包括答案和解析)
|
分离和提纯的方法 |
分离的物质 |
应注意的事项 |
应用举例 |
|
过滤 |
用于固液混合的分离 |
一贴、二低、三靠 |
如粗盐的提纯 |
|
蒸馏 |
提纯或分离沸点不同的液体混合物 |
防止液体暴沸,温度计水银球的位置,如石油的蒸馏中冷凝管中水的流向 |
如石油的蒸馏 |
|
萃取 |
利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法 |
选择的萃取剂应符合下列要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂 |
用四氯化碳萃取溴水里的溴、碘 |
|
分液 |
分离互不相溶的液体 |
打开上端活塞或使活塞上的凹槽与漏斗上的水孔,使漏斗内外空气相通。打开活塞,使下层液体慢慢流出,及时关闭活塞,上层液体由上端倒出 |
如用四氯化碳萃取溴水里的溴、碘后再分液 |
|
蒸发和结晶 |
用来分离和提纯几种可溶性固体的混合物 |
加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液;当蒸发皿中出现较多的固体时,即停止加热 |
分离NaCl和KNO3混合物 |
5.电离(电解质在水溶液中或熔融状态下产生自由移动的离子的过程)方程式
NaCl == Na+ + Cl- H2SO4 == 2H+ + SO42- NaOH == Na+ + OH-
第二单元 研究物质的实验方法
4.化合物
电解质:在水溶液中或熔融的状态下能导电的化合物
非电解质:在水溶液中或熔融的状态下都不能导电的化合物
3.溶液:电解质溶液、非电解质溶液
2.胶体:
(1)概念:分散质微粒直径大小在10-9~10-7m之间的分散系。
(2)性质:①丁达尔现象(用聚光手电筒照射胶体时,可以看到在胶体中出现一条光亮的“通路”,这是胶体的丁达尔现象。)
②凝聚作用(吸附水中的悬浮颗粒)
1.分散系:一种(或几种)物质的微粒分散到另一种物质里形成的混合物。
分类(根据分散质粒子直径大小):溶液(小于10-9m 〉、胶体(10-9~10-7m)
浊液(大于10-7m)
1、物质的聚集状态:气态、液态和固态
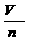 2、气体摩尔体积
2、气体摩尔体积
单位物质的量的气体所占的体积。符号:Vm表达式:Vm= ;单位:L·mol-1
在标准状况下,1 mol任何气体的体积都约是22.4 L。
2、数学表达式:
1、定义:1mol任何物质的质量,称为该物质的摩尔质量。用符号:M表示,常用单位为g·mol-1
5.、

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com