
题目列表(包括答案和解析)
1. 酸性 2. 氧化性 3. 漂白性 4. 不稳定性
Cl-的检验:试剂:AgNO3溶液和稀硝酸 现象:产生白色沉淀(不溶于稀硝酸)
结论:溶液中有Cl-
次氯酸的性质
3. Cl2与碱的反应
氯气 + 碱 → 次氯酸盐 + 金属氯化物 + 水
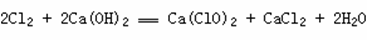
氯水

成分 分子:H2O、Cl2、HClO 离子:H+、Cl-(还有ClO-、OH-)
氯水的性质
2. Cl2与非金属反应
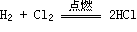
1. Cl2与金属反应(一般将金属氧化成高价态)
Cl2与金属反应(一般将金属氧化成高价态)
6. 溶解性:溶于水(1 : 2)
化学性质
物理性质
1. 颜色:黄绿色2. 气味:刺激性气味3. 状态:气态4. 毒性:有毒5. 密度:比空气大
|
|

 表示质量数为A、质子数为Z的具体的X原子。
表示质量数为A、质子数为Z的具体的X原子。
|

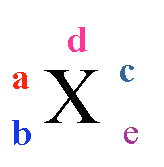

质量数(A)=质子数(Z)+中子数(N)
(1) 原子:核电荷数(质子数)=核外电子数,
(2) 阳离子:核电荷数(质子数)>核外电子数,
(3) 阴离子:核电荷数(质子数)<核外电子数,
核素:具有一定质子数和一定中子数的一种原子。
同位素:质子数相同、质量数(中子数)不同的原子(核素)互为同位素
专题二 从海水中获得的化学物质
第一单元 氯、溴、碘及其化合物
|
2NaCl + 2H2O ==== 2NaOH + H2↑ + Cl2↑
负极 正极
近代原子结构模型的演变
|
模型 |
道尔顿 |
汤姆生 |
卢瑟福 |
玻尔 |
量子力学 |
|
年代 |
1803 |
1904 |
1911 |
1913 |
1926 |
|
依据 |
元素化合时的质量比例关系 |
发现电子 |
ɑ粒子散射 |
氢原子光谱 |
近代科学实验 |
|
主要内容 |
原子是不可再分的实心小球 |
葡萄干面包式 |
含核模型 |
行星轨道式原子模型 |
量子力学 |
1. 核外电子排布规律:
(1) 核外电子总是尽先排布在能量较低的电子层,然后由里向外,排布在能量较高的电子层
(2) 原子核外各电子层最多容纳2n2个电子(表示电子层数)。
(3) 原子最外野电子数目不能超过8个(第一层不能超过2个)
(4) 次外层电子数目不能超过18个(第一层为次外层时不能超过2个),倒数第三层电子数目不能超过32个。




2.物质的量的浓度的配制:计算、称量(或量取)、溶解、转移、洗涤、定容、摇匀、装瓶贴签
具体步骤:
(1)计算:固体物质计算所需质量,液体物质计算所需体积;
(2)称量(量取):固体用天平,液体用量筒;
(3) 溶解(稀释):将固体(溶液)转移至烧杯中,用适量的蒸馏水溶解(稀释),冷却到室温;
(4) 转移:将烧杯中的溶液有玻璃棒小心地引流到(适当规格的)容量瓶中:
(5) 洗涤:有蒸馏水洗涤烧杯内壁2~3次,并将每次洗涤的溶液都注入到容量瓶;
(6)定容:缓缓地将蒸馏水注入到容量瓶中,直到容量瓶中的液面接近容量瓶的刻度线1~2 cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面正好与刻度线相切;
(7)摇匀:将容量瓶盖好,反复上下颠倒,摇匀;
(8)装瓶。
第三单元 人类对原子结构的认识
1.物质的量的浓度 C(B)= n(B)/V(溶液)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com