
题目列表(包括答案和解析)
10.(1) 加热分解法:取两种少许待检粉末于试管中,分别加热,有CO2气体产生的是NaHCO3。
(2)盐酸产气法:取两种少许待检粉末于试管中,同时分别在两支试管中加入1mL稀盐酸,产气速度快的是NaHCO3。
(3)焰色反应法:取两种粉末进行焰色反应实验,透过钴玻璃能够观察到紫色火焰的是K2CO3 。
8. 2 NaHCO3 = Na2CO3+ CO2↑+ H2O 通人过量的CO2
CO32-+ CO2 +H2O= 2HCO-3 ;试剂是 饱和的NaHCO3溶液 ,反应的离子方程式为 HCO-3+H+=H2O+CO2
1.B 2.A 3.BD 4. D 5.C 6.B 7.D
12.现有Na2CO3和NaHCO3的混合物13.7g,用过量的盐酸处理,共收集到气体6.6g,求混合物中NaHCO3的质量分数。
苏教版必修1专题2 第二单元课时练习2 碳酸钠的性质与应用答案
11.工业生产的纯碱中常含有少量的NaCl杂质。某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用下图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数。
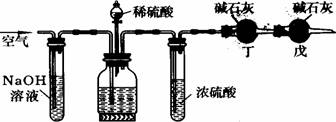
甲 乙 丙
(1)甲装置的作用是 ;丙装置的作用是
(2)乙装置反应前先通数分钟空气的作用是 ,甲装置反应的离子方程式是 。
(3)若去掉丙装置,测得的CO2质量会 (填“偏大”或“偏小”)。
(4)若取ng样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为mg,实验结束后称得干燥管丁的总质量为w,则Na2CO3质量分数的计算式为 。
10.(8分)有两包白色粉末,只知分别是K2CO3和NaHCO3,请你写出鉴别方法(可以少于2种,也可以多于2种,写出2种方法可得6分,3种以上方法得8分)?
⑴ 。
⑵ 。
⑶ 。
9.Na2CO3固体中混有少量NaHCO3,除去杂质的方法是 ,反应方程式为 ;NaHCO3溶液中混有少量Na2CO3,除去杂质的方法是 ,反应的离子方程式为 ;除去CO2气体中少量HCl,所用试剂是 ,反应的离子方程式为 。
8.碳酸钠俗名________或________,是一种________色________体,含10个结晶水的碳酸钠的化学式________________,写出碳酸钠与盐酸反应的离子方程式_______。
7.一定温度下,向足量的饱和Na2CO3溶液中加入1.06g无水Na2CO3,搅拌后静止,最终所得晶体的质量是 ( )
A.等于1.06g B.大于1.06g而小于2.86g C.等于2.86g D.大于2.86g
6.有相同质量的两份NaHCO3粉末,第一份加入足量盐酸,笫二份先加热使其完全分解再加足量同质量分数的盐酸,则两者所消耗的盐酸中氯化氢的质量比为 ( )
A.2:1 B.1:1 C.1:2 D.4:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com