
题目列表(包括答案和解析)
3.某些不合格的建筑装饰材料,会缓慢释放出浓度过高、影响健康的气体,这些气体最常见的是 ( )
A.二氧化氮 B.二氧化硫
C.一氧化碳
D.甲苯等有机物蒸气和甲醛
2.天然皮革是 ( )
A.纤维素制品 B.脂肪类物质
C.橡胶制品 D.凝固和变性的蛋白质
1.化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化不属于化学反应的是 ( )
A.天然气燃烧 B.金刚石变成石墨
C.氯化钠熔化 D.五氧化二磷吸水
25.丙酮和碘在酸性溶液中发生下列反应:CH3COCH3+I2 → CH3COCH2I +H+ +I-。 25℃ 时,该反应的速率由下列经验式决定:v=2.73×10-5c(CH3COCH3)c(H+) mol/(L•s)。25℃时,如果c(I2)、c(CH3COCH3)、c(H+)的起始浓度依次是0.01mol/L、0.1mol/L、0.01mol/L,求:
(1)反应开始时的速率是多少?
(2)当溶液中的I2消耗一半时,反应速率比开始时慢还是快?
24.(8分)天然气是一种重要的化石燃料,起主要成分是甲烷。
(1)甲烷分子的空间构型是
(2)甲烷和氯气在光照条件下可以发生取代反应,写出甲烷和氯气发生一取代的反应方程式
(3)1mol甲烷和一定量的氯气反应生成了四种物质的量相等的取代产物。则上述反应中消耗氯气的物质的量是
(4)天然气作为燃料具有热值大、污染小等优点,作为西部大开发的重点工程---西气东输,将为中部和广大长三角地区提供清洁的天然气,如果你家里现在用的液化石油气(主要成分C3H8)改用天然气,你只要将现在家用燃气灶具做适当的改进就可安全使用天然气。你准备采用什么方法来改进?
23.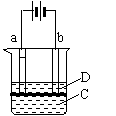 (12分)由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,应用下图电解实验可以制得白色的纯净的Fe(OH)2沉淀,两电极材料分别为石墨和铁。
(12分)由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,应用下图电解实验可以制得白色的纯净的Fe(OH)2沉淀,两电极材料分别为石墨和铁。
(1)a电极材料应为 ,电极反应式为
(2)电解液C可以是 (填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2
(3)D为苯,其作用是 ,在加入苯
之前对C应作何简单处理
(4)为了在较短时间内看到白色沉淀,可采取的措施是(填编号)
A.该用稀硫酸作电解液 B.适当增大电源电压
C.适当减小两电极间的距离 D.适当降低电解液的温度
(5)若C中用Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为 。
22.(14分)W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。由此可知:
(1)写出元素符号:W为 ,X为 ,Y为 , Z为 。
(2)W 2Z的电子式为 。
(3)由Y、X、W组成的物质中含有 键和 键。
21.(6分)写出下列微粒的电子式
(1)H2O (2)Cl- (3)NH4+
20.下面四个选项是四位同学在学习过化学反应速率和化学平衡理论以后,联系化工生产实际所发表的看法,你认为不正确的是 ( )
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.化学反应速率理论可指导怎样提高原料的转化率
C.化学平衡理论可指导怎样使用有限原料多出产品
D.利用化学反应速率和化学平衡理论可提高化工生产的综合经济效益
19.人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变成Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有 ( )
A.酸性 B.碱性 C.氧化性 D.还原性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com