
题目列表(包括答案和解析)
25.(5分)某元素R的最高价氧化物的水化物的化学式为HROx,气态氢化物的化学式为HyR,已知1 mol HROx比HyR质量多64 g,又知 1mol HROx中R的核内质子数比1 mol HROx中氢、氧原子核内质子总数少16 mol,试求R的原子序数。
24.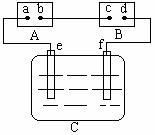 (11分)右图中A是直流电源,B是浸透滴有酚酞的饱和食
(11分)右图中A是直流电源,B是浸透滴有酚酞的饱和食
盐水溶液的滤纸,C为盛有稀硫酸的电解槽,e、f为铂电
极。接通电路一段时间后,发现B上的c点显红色。试回
答:
(1)电源A上的b为 极
(2)写出B上的电极反应
阳极
阴极
总反应
(3)e、f电极上所产生的气体各为 和 ,其体积比是 。
23.(12分)不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。
下面是某些短周期元素的x值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x值 |
0.98 |
1.57 |
2.04 |
2.25 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
(1)通过分析x值变化规律,确定Mg、N的x值范围:
<x(Mg)< , <x(N)< 。
(2)推测x值与原子半径的关系是 。
据据短周期元素的x值变化特点,体现了元素性质的 ____ 变化规律。
22.(14分)短周期元素X、Y、Z组成的化合物Y2X和ZX2。Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3。已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子的最外层电子数是次外层电子数的2倍。试回答:
(1)X、Y、Z元素的名称及符号:X__ __、__ __。Y__ ___、___ _。Z_____、_____。
(2)用电子式表示ZX2化学键的形成过程____________ ______________________。
(3)Y2X对应水化物的电子式为 _ ______,其中存在的化学键有 _______________。
(4)写出Y2X溶于水的溶液与ZX2反应生成化合物Y2ZX3的离子方程式____________。
21.(8分)已知1mol CO气体完全燃烧生成CO2气体,放出283kJ热量,1mol氢气完全燃烧生成液态水放出286kJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890kJ热量,
(1)写出H2完全燃烧生成液态水的热化学方程式________________________________
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量_______890kJ(填“ =”、“>”、“<”)
(3)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)的取值范围是______________________________________
(4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物质的量相等,则放出热量(Q)的取值范围是________________________________
20.(8分)(1) 溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在
溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在 的水溶液中存在如下平衡:
的水溶液中存在如下平衡: 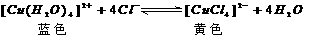
现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法:
(1)____________________________,(2)___________________________。
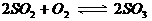 (2)在
的平衡体系中,加入
(2)在
的平衡体系中,加入 构成氧气,当平衡发生移动后,
构成氧气,当平衡发生移动后, 中
中 的含量_________(填增加、减少或不变),其原因是_________________________________。
的含量_________(填增加、减少或不变),其原因是_________________________________。
19.(8分)在下列物质中:(1)含离子键的物质是_____________;(2)既有离子键又有共价键的化合物是__________;(3)由极性键形成的非极性分子是__________ ;(4)由非极性键形成的非极性分子是____________;(选填序号)
(A)Cl2、 (B)NaOH、 (C)H2S、 (D)CO2、 (E)CaCl2、
(F)N2、 (G)CCl4、 (H)NH4Cl、 (I)NH3、 (J)HBr
18.将固体NH4Br置于密闭容器中,在某温度下,发生下列反应:

 NH4Br(s) NH3(g)+HBr(g);2HBr(g) Br2(g)+H2(g)
NH4Br(s) NH3(g)+HBr(g);2HBr(g) Br2(g)+H2(g)
2 min后,反应到达平衡,测知C(H2)=0.5mol/L,C(HBr)=4mol/L.若用V(NH3)表示NH4Br的分解反应速率,下列速率正确的是 ( )
A.0.5mol/ (L· min) B.2.5 mol/ (L·min) C.2 mol/ (L· min) D.5 mol/ (L ·min)
第II卷(非选择题,共78分)
17.同一周期的X、Y、Z三种元素,已知其最高价氧化物的水化物的酸性由强到弱的顺序是:HZO4>H2YO4>H3XO4,下列说法错误的是 ( )
A.它们的原子半径按X、Y、Z的顺序增大
B.非金属性按X、Y、Z的顺序减弱
C.它们的气态氢化物的稳定性按X、Y、Z顺序增强
D.三种元素阴离子的还原性按X、Y、Z顺序减弱
16.在电解水制取H2和O2时,为了增强导电性,常常加入一些电解质,最好选用下列物质中的 ( )
A.NaOH B.HCl C.NaCl D.CuSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com