
题目列表(包括答案和解析)
16、(6分)将20g Ba(OH)2•8H2O固体与10g NH4Cl晶体在烧杯中混合,不断搅拌,实验现象为:
,
该反应的化学方程式:
15、(6分)芒硝(Na2SO4•10H2O)是重要的化工原料,具有广泛的用途。芒硝可调节室内温度,科学家利用太阳能的方法之一,是将装有芒硝的密闭聚乙烯管安装在房屋的外墙内,当太阳照射时,它能将太阳能转化为化学能,达到蓄热效果,使室内保持较低温度;晚上,它能将化学能转化为热能,使室内保持温度。请结合方程式解析其原因。
14、在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
A、0.1mol.L-1.min-1 B、0.2mol.L-1.min-1
C、0.3mol.L-1.min-1 D、0.6mol.L-1.min-1
13、下列变化是因原电池反应而引起的是
A、在空气中金属铝表面迅速氧化形成保护膜
B、常温下,铁被浓硫酸“钝化”形成保护膜
C、在潮湿的空气中钢铁易生锈 D、在潮湿的空气中过氧化钠易变质
12、下列实验中,反应速率加快是由催化剂引起的是:
A、在炭粉中加入KClO3,点燃时燃烧更为剧烈
B、锌与稀硫酸反应中加入少量CuSO4溶液而使反应放出H2的速率加快
C、固态FeCl3和固体NaOH混合后,加入水能迅速产生沉淀
D、双氧水中加入少量MnO2,即可迅速放出气体
11、在反应:C + CO2 ≒ 2CO中,可使反应速率增大的措施是:
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强
A、①②③④ B、②③④⑤ C、①②③ D、②③④
10、可逆反应2SO2
+ O2 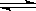 2SO3达到平衡的标志是
2SO3达到平衡的标志是
① 消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③ 反应混合物中,SO3的质量分数不再改变
A、①② B、①③ C、只有③ D、只有①
9、X,Y,Z都是金属,把X浸入Z的硝酸盐溶液中,X表面有Z析出,X与Y组成原电池时,Y为负极。X,Y,Z三种金属的活动性顺序为:
A、X>Y>Z B、X>Z>Y C、Y>X>Z D、Y>Z>X
8、已知空气――锌电池的电极反应为:
锌片:Zn + 2OH- - 2e- = ZnO + H2O
石墨:O2 + 2H2O + 4e- = 4OH-
根据此判断,锌片是:
A、负极,并被氧化 B、负极,并被还原
C、正极,并被氧化 D、正极,并被还原
7、废电池的污染引起人们广泛注意,废电池对环境造成污染的主要物质是:
A、锌 B、汞 C、石墨 D、二氧化锰
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com