
题目列表(包括答案和解析)
8.近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80Mpa下合成出了金刚石,具有深远的意义。下列说法错误的是 ( )
A.由二氧化碳合成金刚石是氧化还原反应
B.该反应中二氧化碳完全被还原为金刚石
C.钠被氧化最终生成碳酸钠
D.金刚石是碳的一种同素异形体
7.下列关于碳酸钠和碳酸氢钠的比较中,正确的是 ( )
A .二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度
B .二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性
C.二者都能与盐酸反应放出二氧化碳气体,但产气量和反应快慢不同
D .二者在一定的条件下可以相互转化
6.下列关于“焰色反应”的理解正确的是 ( )
A.只有金属单质才有焰色反应
B.只有金属化合物才有焰色反应
C.只有某些金属或其化合物才有焰色反应
D.只有金属离子才有焰色反应
5.下列操作中,溶液的颜色不发生变化的是 ( )
A.碳酸氢钠溶液中滴加稀盐酸 B.硫酸铁溶液中滴加硫氰化钾溶液
C.碘水中滴加淀粉碘化钾溶液 D.氯化铁溶液中加入还原性铁粉
4.随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品氧化变质,在包装袋中可以放入的化学物质是 ( ) A.无水硫酸铜 B.硫酸亚铁 C. 食盐 D. 生石灰
3.下列物质露置在空气中,质量会减轻的是 ( ) A.NaOH B.Na 2O2 C.无水CaCl2 D.Na2CO3·10H2O
2.氢氧化铝可作为治疗某种胃病的内服药,这是利用了氢氧化铝的哪个性质 ( ) A.酸性 B.碱性 C.两性 D.氧化性
1.对氧化铝的分类中正确的是 ( )
A.酸性氧化物 B.碱性氧化物
C.两性氧化物 D.不成盐氧化物(像CO一样)
14.2:7
解析:在FeCl3和CuCl2的混合溶液中加入过量的Fe粉后,Fe粉会将Fe3+和Cu2+全部消耗掉。Fe3+与Fe反应会使溶液增重,Cu2+与Fe反应会使溶液减重。依据题意,若反应前后溶液的质量没变,则这两个反应增重与减重必然相等才能符合题意。
设反应前Fe3+为x mol,Cu2+为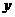 mol,
mol,
2Fe3+十Fe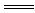 3Fe2+ 增重
3Fe2+ 增重
2 3 56
x 28 x
Cu2+十Fe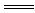 Fe2++Cu 减重
Fe2++Cu 减重
1 1 8
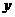 8
8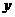
由28 x=8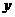 得x:
得x: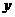 =2:7
=2:7
所以原混合溶液中Fe3+和Cu2+的物质的量之比为2:7
13.方法一:(1)稀H2SO4、铁屑(2)煮沸(3)避免生成的Fe(OH)2沉淀接触O2
方法二:(1)稀H2SO4、铁屑(2)NaOH溶液(3)检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯净时,再夹紧止水夹(4)试管Ⅰ中反应生成的H2充满了试管I和试管Ⅱ,且外界空气不容易进入
解析:方法一中根据FeSO4具有易被氧化和易水解的特点,在配制其溶液时还需加入稀H2SO4和铁屑;蒸馏水中若溶有O2,则会加速Fe(OH)2氧化,因此可采用煮沸法除去O2。为避免生成的Fe(OH)2沉淀接触O2,可用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液方可达到目的。
方法二的原理是利用稀H2SO4和铁屑产生氢气,先赶净装置中空气。确定赶净空气后再夹紧止水夹,通过H2产生的压强将FeSO4压入NAOH溶液中去,从而使产生的白色Fe(OH)2沉淀在H2的还原性气氛中得以较长时间保持。
点评:这是一道与Fe(OH)2的制备原理有关的题目,采用了创新的实验手法。对此类题目的完美解答,有赖于对基础知识的扎实掌握,对有关实验原理和仪器的熟知程度,并需要大胆的开拓和创新精神。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com