
题目列表(包括答案和解析)
27.(10分)使一定质量的锌与100mL18.5mol/L浓H2SO4充分反应,锌完全溶解,同时生成气体A 33.6L(标准状况下)。将反应后的溶液稀释至1L,测得溶液c(H+)为0.1mol/L,求:
(1)气体A中各成分的物质的量分别是多少?
(2)若往反应后的溶液中加入足量的BaCl2溶液,则所生成的BaSO4沉淀的物质的量为多少?
(提示:Zn+2H2SO4(浓) == ZnSO4+SO2↑+H2O,浓H2SO4与Zn反应时,随着反应的进行H2SO4由浓逐渐变稀、相应生成的气体也不同)
26.(5分)将标准状况下336LHCl气体溶于1L水中,所得盐酸溶液的密度为1.18g·cm-3。求该盐酸的物质的量浓度。
25.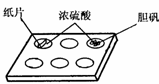 (18分)某学生做浓硫酸性质的实验:
(18分)某学生做浓硫酸性质的实验:
实验一:在一个白色的点滴板的孔穴中分别放入小纸片、
少量CuSO4·5H2O。然后如图所示,分别滴入几滴浓硫酸,
观察现象。回答下列问题:
(1)浓硫酸滴在小纸片上,小纸片变 (填实验现象),说明浓硫酸具有 性。
(2)浓硫酸滴入CuSO4·5H2O中,胆矾 (填实验现象),说明浓硫酸具有 性。
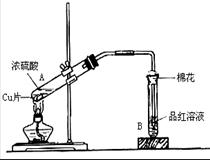 实验二:用如右图装置进行铜与一定体积已知浓
实验二:用如右图装置进行铜与一定体积已知浓
度的浓硫酸反应的实验研究。
(1)写出试管B中的实验现象 。
(2)写出A处反应的化学方程式,并用双线桥
标明电子转移的方向和数目:
。
(3)充分反应后,该学生发现铜和硫酸都有剩余。在不补充浓硫酸的前提下,若要使剩余的铜片溶解,可再加入(要求填写一种与硫酸不同类别的物质) 。
(4)B试管口的棉花应沾有的试剂是 。
24.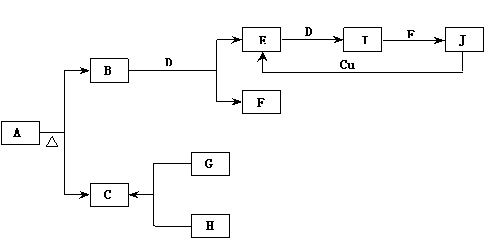 (11分)已知:(1)A为正盐。(2)常温、常压下,B、C、D、E、G、H、I均为气体,其中D、G、H为单质,H为黄绿色气体,I通常为红棕色气体。(3)F在常温下是一种无色液体。(4)C、J的水溶液是一种酸。图中反应条件(除加热外)均已略去。
(11分)已知:(1)A为正盐。(2)常温、常压下,B、C、D、E、G、H、I均为气体,其中D、G、H为单质,H为黄绿色气体,I通常为红棕色气体。(3)F在常温下是一种无色液体。(4)C、J的水溶液是一种酸。图中反应条件(除加热外)均已略去。
(1)写出A的化学式:A 。
(2)写出下列反应的化学方程式:
①B + D → E + F : ;
②J + Cu → E: ;
③H和石灰乳的反应: 。
(3)在I和F的反应中,氧化剂和还原剂的质量比为: 。
23.(4分)配平下列化学方程式,并指出其中的还原剂:
H2S + HNO3(浓) -- H2SO4+ NO2↑+ H2O,还原剂是 。
22.(6分)写出除去下列物质中所混有的少量杂质的有关的离子方程式:
(1)CuO中混有少量Al2O3 ;
(2)FeCl2溶液中混有少量FeCl3 。
21.(6分)用化学方程式解释下列有关的现象:
(1)过量的二氧化碳通入偏铝酸钠溶液中,产生白色沉淀:
;
(2)久置的浓硝酸变黄: 。
20.将2.56gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为 ( )
A.0.05 mol B.1mol C.1.05mol D.0.13mol
19.两份铝片,一份与足量盐酸反应,另一份与足量烧碱溶液反应,同温、同压下,放出相同体积的气体,则两份铝片的质量之比为 ( )
A.1∶1 B.2∶3 C.3∶2 D.1∶6
18.下列四组实验,根据实验事实得出的结论,正确的是 ( )
A.在某试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀硝酸不溶解--原未知试液中一定含有SO42-
B.某未知气体在空气中燃烧,其产物能使无水CuSO4变蓝色--原气体一定是H2
C.在某未知试液中滴加盐酸产生无色气体,将该气体通入足量澄清石灰水中得白色沉淀--原未知试液中一定含有CO32-
D.在某未知试液中加入浓的NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体--原未知试液中一定含有NH4+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com