
题目列表(包括答案和解析)
1我们学过一首数字小诗,里面藏着十个数字,还记么?
齐诵“一去二三里,……”
2请五位同学上台板书一到十,每个人两个。
3别小看这些数字,它让我们学到了好多基本笔画。师一
一指出,指名学生说。
23.在一定条件下,NO和NH3可以发生如下反应6NO+4NH3=5N2+6H2O,现有NO和NH3的混合物1mol,充分反应后所得产物中,若经还原得到的N2比经氧化得到的N2多1.4g。
求: 若以上反应进行完全,试计算原反应混合物中NO与NH3的物质的量可能各是多少?
22.(11分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置先进行了有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整。
(2)实验中他们取6.4g铜片和12mL
18mol·L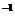 浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜跟浓硫酸反应的化学方程式:_____________________________________。
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是:
________________________________________________________________。
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是_____(填写字母编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)为定量测定余酸的物质的量浓度,某学生进行了如下设计:
先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度。他认为测定SO2的量的方法有多种,请问下列实验方案中不可行的是_______(填写字母编号)。
A.将装置A产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量的硫酸酸化的KMnO4溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.用排饱和NaHSO3溶液的方法测出装置A产生气体的体积(已折算成标准状况)
(4)如果(3)中测得标准状况下产生SO2的体积为1.792L,则被还原的硫酸的物质的量为 mol。
21.(10分)从某物质A的水溶液出发有如图所示的转化关系,
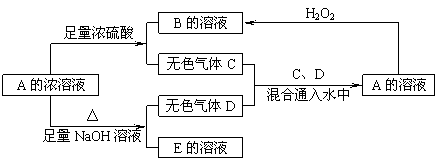
其中A为正盐,气体C能使品红溶液褪色,气体D能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)写出A的化学式: _________,D的结构式____________。
(2)写出下列反应的离子方程式
①A与足量NaOH溶液(加热)_____________________ _。
②C、D通人水中:_____________ 。
(3)检验B溶液中阴离子的实验操作和实验现象是___________________________________ 。
20.(12分)下面是元素周期表的一部分,针对①-⑩元素填写下列空白
|
主族 周期 |
IA |
|
O |
|||||
|
1 |
① |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
|
|
2 |
|
|
|
② |
|
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)在这些元素中,属于金属元素的有________________(填元素符号)
(2)画出⑦元素原子结构示意图______________________________
(3)写出①和⑩形成的化合物的电子式_______________________
(4)用电子式表示④和⑥形成化合物的过程 。
(5)写出①和②的最低价形成气态分子的化学式______________,
判断分子为 。(填极性分子或非极性分子)
(6)根据NaH的存在,有人提议可把氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的 族。
19.(4分)有以下几种物质,按要求填写物质代号:
A.金刚石 B.D2O C.126C D.C60 E.Na2O2 F.H2O
G.CO2 H.146C I.NaOH J.147N
(1) 属于同素异形体的是____________
(2)互为同位素的是______________
(3)含有极性键的离子化合物的是_____________
(4)既含有非极性共价键又含有离子键的是____________
18. 向25mL18.4mol/LH2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量是 ( )
A.小于0.23mol B.等于0.23mol C.0.23mol~0.46mol之间 D.等于0.46mol
第Ⅱ卷(共46分)
17. 向BaCl2溶液中通入SO2没有沉淀生成。但若先加入一种试剂,再通入SO2,则可看到沉淀生成,这种试剂可能是:①NH3 ②NaOH ③HCl ④CO2 ⑤Cl2。 ( )
A.①②④ B.②③ C.④⑤ D.①②⑤
16. 下列指定微粒的个数比为2:1的是 ( )
A.Be2+离子中的质子和电子
B.21H原子中的中子和质子
C.NaHCO3晶体中的阳离子和阴离子
D.BaO2(过氧化钡)固体中的阴离子和阳离子
15.下列变化的实质相似的是: ( )
A.浓H2SO4和浓HCl在空气中敞口放置时浓度均减小. B.SO2和Cl2均能使品红溶液褪色. C.浓H2SO4和稀硫酸与锌反应均生产气体. D.HBr,HI气体不能用浓H2SO4制取
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com