
题目列表(包括答案和解析)
5. 下列变化过程中,共价键被破坏的是
A. 烧碱溶于水 B.氯化氢气体溶于水 C.二氧化碳变成干冰 D.碘溶于酒精
4. 元素的以下性质,随着原子序数递增不呈现周期性变化的是
A.相对原子质量 B.化合价 C.元素的金属性和非金属性 D.原子半径
3.下列表示物质结构的化学用语或模型正确的是
A.8个中子的碳原子的核素符号:12C B.HF的电子式: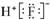
C.Cl-离子的结构示意图: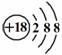 D. 次氯酸的结构式: H-O-Cl
D. 次氯酸的结构式: H-O-Cl
2.美国与俄罗斯科学家于2006年成功地合成了3个118号超重元素原子并观察到其存在。这种超重元素只能持续存在极短的时间,约有0.9毫秒,之后即迅速衰变为原子量较小的其它元素。下列有关说法正确的是
A. 118号元素的原子核中含有118个质子
B.118号元素是一种金属元素
C. 118号元素属于第八周期元素
D.118号元素原子经化学反应后可转化成其它元素的原子
1. 中共十七大报告提出:“建设生态文明,基本形成节约能源资源和保护生态环境的产业结构、增长方式、消费模式”。下列行为不利于“生态文明”建设的是
A.把环境保护作为奥运设施规划和建设的首要条件
B.推广“低碳经济”,减少温室气体的排放
C.开发可再生能源,合理使用化石燃料,提高能源利用率
D.推进小煤矿、小火力电站的兴建,促进地方经济的快速发展
29.(6分)把4 mol N2和8 mol H2置于5 L密闭容器合成氨反应,达到平衡时测得混合气体中含NH3的体积百分比为20%,求:(1)混合气体中含H2的体积百分比;
(2)反应前后容器内的压强比; (3)N2和H2的转化率。
28.(6分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
|
时间(min) |
1 |
2 |
3 |
4 |
5 |
|
氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
① 哪一时间段(指0-1、1-2、2-3、3-4、4-5 min)反应速率最大 ,原因是
② 哪一段时段的反应速率最小 ,原因是 。
③ 求2 ~ 3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,要写出计算过程。
27、(8分)已知电极材料:铁、铜、银、石墨、锌、铝,电解质溶液:氯化铜溶液、硫酸铁溶液、盐酸。按要求回答下列问题:
①电工操作上规定:不能把铜导线和铝导线连接在一起使用,请说明原因。
。
②若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? ,若能,请写出电极反应式,负极 ,
正极 。若不能后面两空不填。
③有M、N两种金属分别与稀盐酸反应,产生氢气速率相近,请设计一个实验证明M、N两种金属的活泼性 。
26.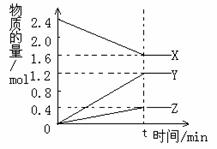 (6分),在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如右图。反应在t时到达平衡,依图所示:
(6分),在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如右图。反应在t时到达平衡,依图所示:
(1)该反应的化学方程式是 。
(2)反应起始至t,Y的平均反应速率是 。
(3)X的物质的转化率是 。
(4)生活中利用原电池原理生产了各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其主要原因是 。
A、回收利用电池外壳的金属
B、防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
C、防止电池中渗泄的电解液腐蚀其他物品 D、回收其中石墨电极
25.(4分)拆开1mol H-H键,1mol N-H键,1mol N三N键分别需要吸收的能量为436kJ ,391kJ,946kJ:则1mol N2生成NH3 热量(填:吸收或放出) kJ;
理论上,每生成1mol NH3, 热量(填:吸收或放出) kJ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com