
题目列表(包括答案和解析)
27、(8分)(1)未用玻璃棒引流; 未采用200 mL容量瓶。
(2)砝码放在左盘,烧杯放在右盘(或砝码和物品的位置放反了);
(3) A
23 (8分) ( 1)3Cu+8H++2 NO3-=3Cu2++2NO↑+4H2O
(2)25 1.806×1024(3×6.02×1023;3NA) 96
24. (6分) (1)2Al+3I2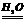 2AlI3 (2)出现紫色蒸气 (3)催化剂
2AlI3 (2)出现紫色蒸气 (3)催化剂
25(7分). 1)Cu , CuCl2 , Cu(OH)2 ,CuO (若写成名称扣2分)
 2) a)
Cu+Cl2 △ CuCl2 (若没注明条件扣1分,没配平不给分)
2) a)
Cu+Cl2 △ CuCl2 (若没注明条件扣1分,没配平不给分)
b) Fe+ CuCl2=Cu+FeCl2
26(7分)( 1). 2F2+2H2O=4HF+O2
( 2) Ca(ClO)2+CO2+H2O=CaCO3+2HclO(此方程正确可给3分) 2HClO====2HCl+O2↑。
( 3) 2Na2O2+2CO2=2Na2CO3+O2 氧气
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
D |
B |
A |
D |
A |
A |
B |
C |
B |
A |
A |
|
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
|
D |
B |
A |
D |
D |
C |
C |
B |
B |
B |
C |
31.(6分)把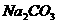 和
和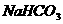 的混合物29.6g加热到质量不再变化时,得残留固体26.5g。求原混合物中
的混合物29.6g加热到质量不再变化时,得残留固体26.5g。求原混合物中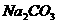 与
与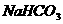 的物质的量之比。
的物质的量之比。
垫江师范高2010级高一化学上期期末复习试题二
答案及评分说明
30、状准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液,(1)求所得盐酸的物质的量浓度?
(2)若将此溶液再稀释成1L溶液,求稀释后盐酸的物质的量浓度?
(3)将(2)的溶液取出250mL与足量的Zn反应可以产生多少体积的H2(在标准状况下) ? (8分)
29. 甲烷(CH4)与氧气的混合气体在标况下的密度为1.25g/L,则混合气体中甲烷与氧气的体积比为_______
28.(9分) 过碳酸钠和盐酸反
应的化学方程式为:
2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O,商品
过碳酸钠中一般都含有Na2CO3,为了测定它的
纯度,取一定量的样品和盐酸反应,通过测量
产生的氧气的体积,可以计算出过碳酸钠的含量。
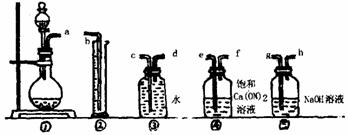 (1)根据下图提供的仪器装置,组装一套测定商品过碳酸钠的实验装置,这些装置的连接顺序是(填接口字母):
。
(1)根据下图提供的仪器装置,组装一套测定商品过碳酸钠的实验装置,这些装置的连接顺序是(填接口字母):
。
(2)装置④的作用: 。
(3)如果实验时,称取wg样品和过量盐酸反应后,没得氧气的体积(标准状况)为VmL,则此样品的纯度为 。
(4)某次实验,称取0.9g样品进行测定,实验室有50mL,100mL,150Ml三种规格的量筒,应选用规格为 的量筒进行实验。
27、(8分)(1)为检验精盐纯度,需配制200 mL 0.2 mol·L-1 NaCl(精盐)溶液,题右图是该同学转移溶液的示意图,图中的两个错误是:______________________;
__________________________________。
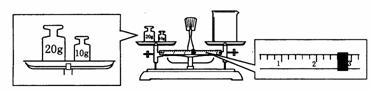 (2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该同学在操作时的一个错误是__________________________________。
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该同学在操作时的一个错误是__________________________________。
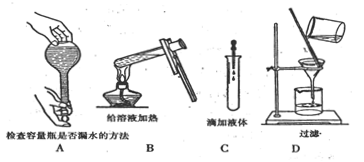 (3)下列实验操作
(3)下列实验操作
与方法正确的是__________(填A,B,C,D序号)
32.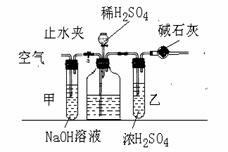 (10分)工业生产的纯碱中常含有少量的NaCl等杂质。下图是测定产品中碳酸钠质量分数的实验装置。实验步骤有(有的步骤可能重复):
(10分)工业生产的纯碱中常含有少量的NaCl等杂质。下图是测定产品中碳酸钠质量分数的实验装置。实验步骤有(有的步骤可能重复):
A.在干管中填满碱石灰,质量为mg;
B.取ng样品装入广口瓶中; C.检验装置的气密性;
D.缓缓鼓入空气数分钟,再称干燥管质量为wg;
E.关闭止水夹; F.打开止水夹;
G.缓缓加入稀硫酸到不再产生气体为止;
H.缓缓鼓入空气数分钟。
(1)正确操作顺序是(填写符号)
C 、 、F 、E 、G 、D
 (2)装置甲的作用是
;装置乙的作用是
;
(2)装置甲的作用是
;装置乙的作用是
;
(3)操作步骤D中,要缓缓鼓入空气数分钟,鼓入空气的作用是 ;
(4)溶液中碳酸钠的质量分数的计算式为: ;
(5)若去掉装置甲,测定结果为 ;若去掉装置乙,测定结果为 ;(填“偏大”、“偏小”、或“无影响”)
(6)请再设计一种测定碳酸钠质量分数的方案,并以简要的文字说明实验操作过程。
。
31. (10分)有下图所示的反应关系,A是中学常见的无机物,A、B、C中含有同一种元素R,不含R的产物和水已经略去。
(10分)有下图所示的反应关系,A是中学常见的无机物,A、B、C中含有同一种元素R,不含R的产物和水已经略去。
(1)若A与NaOH反应,既可只生成B, 又可只生成C,还可生成B+C。
①写出两种符合上述反应关系的A的分子式 、 .
②任选上述一种物质,写出有关离子方程式:
生成B的离子方程式为 ;
生成C的离子方程式为 。
(2) 若A与NaOH无论以何种物质的量比反应, 其产物必为B+C,则A的分子式可能是
(只写一种),R在A、 B 、C中的化合价必须满足的条件是 ,
该反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com