
题目列表(包括答案和解析)
11、在一密闭容器中充入一定量的H2和N2,经测定反应开始后3s末的V(H2)=0.3mol/(L•s),则3s末NH3的浓度为:
A、0.4mol/L B、0.6mol/L C、0.9mol/L D、1.2mol/L
10、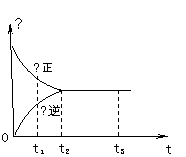 右图是可逆反应X2
+ 3Y2
右图是可逆反应X2
+ 3Y2 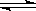 2Z2 在反应
2Z2 在反应
过程中的反应速率(Ʋ)与时间(t)的关系曲线,
下列叙述正确的是
A、t1时,只有正方向反应
B、t2时,反应到达限度
C、t2- t3,反应不再发生
D、t2- t3,各物质的浓度不再发生变化
9、已知可逆反应2SO2 + O2 2SO3,当生成2 mol SO3时放出热量为Q,
 现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则
现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则
A、Q1 = Q B、Q1 < Q C、2Q1 > Q D、无法判断
8、下列措施对增大反应速率明显有效的是:
A、Na与水反应时增大水的用量
B、Fe与稀硫酸反应制取氢气时,改用浓硫酸
C、在K2SO4与BaCl2两溶液反应时,增大压强
D、将铝片改为铝粉,做铝与氧气反应的实验

7、将1mol N2和3 mol H2通入4L的密闭容器中反应,半分钟后测得H2的物质的量为2.1 mol,现用如下三种物质在单位时间内的浓度变化来表示该反应速率。① Ʋ(N2) = 0.15 mol/(L·min) ② Ʋ(N2) = 1.05 mol/(L·min)
③ Ʋ(NH3) = 0.30 mol/(L·min) 其中正确的是
A、①② B、②③ C、①③ D、①②③
6、X,Y,Z都是金属,在X与稀H2SO4反应中,加入少量Z的硫酸盐溶液时能使反应加快;X与Y组成原电池时,Y电极质量减少,X,Y,Z三种金属的活动性顺序为:
A、X>Y>Z B、X>Z>Y C、Y>X>Z D、Y>Z>X
5、氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2 + O2 = 2H2O,正极反应为:O2 + 2H2O + 4e- = 4OH-下列叙述不正确的是
A、 H2通入负极区 B、O2通入正极区
C、负极反应为2H2 + 4OH- - 4e- = 4H2O D、正极发生氧化反应
4、把纯碘化氢气体装入密闭容器中,它将按2HI ≒ H2 + I2反应进行分解(正反应吸热),当系统在趋向平衡状态的过程中,以下描述正确的是:
A、碘化氢的生成速率大于其分解速率
B、碘化氢的生成速率等于其分解速率
C、加催化剂不会影响达到平衡的时间
D、升高温度可以加快平衡状态的到达
3、下列各组中的两个反应,前一个反应放出的热量比后一个反应放出的热量多的是(反应物参与反应的物质的量均按化学方程中的化学计量数计算)
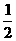 ① 2H2(g)+ O2(g)
= 2H2O(g) 2H2(g)+
O2(g) = 2H2O(l)
① 2H2(g)+ O2(g)
= 2H2O(g) 2H2(g)+
O2(g) = 2H2O(l)
② C(s)+ O2(g) = CO2(g) C(s)+ O2(g) = CO(g)
A、只有① B、只有② C、①② D、①②都不符合题意
2、化学反应的特征是
A、发光发热 B、能量发生变化
C、状态发生变化 D、有新物质生成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com