
题目列表(包括答案和解析)
8.(2007年高考广东化学卷,卤素)氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
(A)若管道漏气遇氨就会产生白烟 (B)该反应属于复分解反应
(C)该反应利用了Cl2的强氧化性 (D)生成1 mol N2有6 mol电子转移
7.下列关于电解质、非电解质的说法正确的是
A、氯气溶于水得氯水,该溶液能导电,因此氯气是电解质
B、CaCO3饱和溶液导电能力很弱,故CaCO3是弱电解质
C、导电能力弱的溶液肯定是弱电解质的溶液
D、HF的水溶液中既有H+、F-,又有大量的HF分子,因此HF是弱电解质
6.下列各组物质,不用任何化学试剂即可鉴别的是 ( )
A. NaCl溶液、NaBr溶液、KI溶液 B. 氯水、NaBr溶液、盐酸
C. 氯化氢、溴化氢、碘化氢 D. 盐酸、NaCl溶液、AgNO3溶液、Na2CO3溶液
5.将19gF2通入81g水中,所得溶液中溶质质量分数是 ( )
A. 19% B. 20% C. 21.7% D. 27.5%
4.向溴化钠、碘化钠的混合溶液中通入足量氯气,之后加热,将溶液蒸干,并灼烧片刻,最后残留的物质是( )
A. NaCl B. NaCl NaBr NaI C. NaBr NaI D. NaI
3.砹是原子序数最大的卤族元素,推测砹的化合物不可能具有的性质是( )
A. 砹是有色固体 B. HAt很稳定 C. AgAt难溶于水 D. 砹易溶于某些有机溶剂
1 (2007年高考理综重庆卷)表中是食用碘盐包装上的部分说明,
下列说法正确的是( )
(A)高温会导致碘的损失 (B)碘酸钾可氧化氯化钠
(C)可用淀粉检验碘盐中的碘酸钾 (D)该碘盐中碘酸钾含量为20 mg/kg-50 mg/kg
2.下列物质的用途与其性质的对应关系错误的是:
A.氯气用于自来水消毒- 次氯酸的强氧化性 B. 碘化银用于人工降雨- 使空气中水蒸汽凝聚
C.氢氟酸腐蚀玻璃- 强酸性 D. 溴化银用于照相术- 光照分解
26.(9分)现有如下两个反应:(A)NaOH + HCl = NaCl + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(1)根据两反应本质,判断能否设计成原电池
(2)如果不能,说明其原因
(3)如果可以,则写出正、负极材料及其电极反应式,电解质溶液名称
。
25.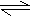 (4分)在密闭容器中发生3X(g)+Y(g)
Z (g)+2W(g)反应,现在控制下列三种不同的条件:
(4分)在密闭容器中发生3X(g)+Y(g)
Z (g)+2W(g)反应,现在控制下列三种不同的条件:
①在400°C时,9molX与3molY反应
②在400°C时,15 molX与5molY反应
③在300°C 时,9molX与3molY反应
那么,反应开始时,正反应速率最大的是(填序号,下同) ,
正反应速率最小的是 。
24.(2分)某反应是吸热反应,且所吸收的热能由外部热源(如酒精灯)提供,提供的热能主要起到 的作用。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com