
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
11ЎўПВБРёч»ҜәПОпөДөзЧУКҪЦРҙнОуөДКЗЈә
ЎЎЎЎЎЎ (A)Na2OЈәNa+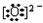 Na+ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (B)CaCl2ЈәCa2+
Na+ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (B)CaCl2ЈәCa2+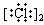
ЎЎ(C)KFЈәK+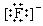 ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (
D)HClЈәH+
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (
D)HClЈәH+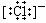
10ЎўФЪФӯөзіШәНөзҪвіШөДөзј«ЙПЛщ·ўЙъөД·ҙУҰЈ¬Н¬КфСх»Ҝ»№Фӯ·ҙУҰ»тН¬Кф»№Фӯ·ҙУҰөДКЗЈә
AЈ®ФӯөзіШөДХэј«әНөзҪвіШөДСфј«Лщ·ўЙъөД·ҙУҰ
BЈ®ФӯөзіШөДХэј«әНөзҪвіШөДТхј«Лщ·ўЙъөД·ҙУҰ
CЈ®ФӯөзіШөДёәј«әНөзҪвіШөДСфј«Лщ·ўЙъөД·ҙУҰ
DЈ®ФӯөзіШөДёәј«әНөзҪвіШөДТхј«Лщ·ўЙъөД·ҙУҰ
9ЎўјЧТТБҪЦЦ·ЗҪрКфРФЦКұИҪПЈ¬УРўЩјЧұИТТИЭТЧУлЗвЖш»ҜәПЈ»ўЪјЧФӯЧУДЬУлТТФӯЧУөДТхАлЧУ·ўЙъСх»Ҝ»№Фӯ·ҙУҰЈ»ўЫЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпЛбРФұИҪПЈ¬јЧұИТТөДЗҝЈ»ўЬУлДіҪрКф·ҙУҰКұјЧФӯЧУөГөзЧУ№ӨТөКэДҝұИТТөД¶аЈ»ўЭјЧөДТфЦКИЫЎў·РөгұИТТөДөНЎЈДЬ№»ЛөГчјЧұИТТөД·ЗҪрКфРФЗҝөДКЗЈә
AЈ® ўЩўЪўЫЎЎЎЎЎЎ BЈ® ўЩўЫўЬЎЎЎЎЎЎЎЎ CЈ® ўЩўЪўЭЎЎЎЎЎЎЎЎЎЎЎЎЎЎ DЈ®ўЩўЪўЫўЬўЭўЮ
8ЎўТ»¶ЁДЬРОіЙАлЧУјьөДКЗЈә AЈ®ҪрКфФӘЛШөДөҘЦКУл·ЗҪрКфФӘЛШөДөҘЦК»ҜәПЎЎЎЎ BЈ®Ц»ПЮУЪўчAәНўсAөДФӘЛШЦ®јд
CЈ®»оЖГөДҪрКфФӘЛШУл»оЖГөД·ЗҪрКфФӘЛШПа»Ҙ»ҜәПDЈ®ИОТвБҪЦЦФӘЛШ»ҜәПҫщҝЙРОіЙАлЧУјь
7ЎўФЪГЬұХөДИЭЖчЦР·ўЙъИзПВҝЙДж·ҙУҰЈәN2 + 3H2 2NH3Ј¬ПВБРІ»ДЬЛөГч·ҙУҰөҪЖҪәвөДКЗЈә
2NH3Ј¬ПВБРІ»ДЬЛөГч·ҙУҰөҪЖҪәвөДКЗЈә
AЈ®ИЭЖчДЪөДС№ЗҝІ»ЛжКұјд¶шұд»ҜЈ»
BЈ®өҘО»КұјдДЪЈ¬ПыәДn mol N2өДН¬КұЈ¬ЙъіЙ2n molNH3ЎЎ Ј»
CЈ®өҘО»КұјдДЪЈ¬ПыәДn mol N2өДН¬КұЈ¬ЙъіЙ3n molH2ЎЎ Ј»
DЈ®ИЭЖчДЪөД»мәПОпөДЧЬОпЦКөДБҝІ»ЛжКұјд¶шұд»ҜЎЈ
6ЎўA әН B КЗН¬ЦЬЖЪөДПаБЪФӘЛШ, B әН C КЗН¬ЦчЧеөДПаБЪФӘЛШ, ЗТAЎўBЎўC ЧоНвІгөзЧУКэЦ®әНОӘ 19,Фт°ҙAЎўBЎўCИэЦЦФӘЛШЛіРтУҰёГКЗЈә
AЈ®NЎў FЎў ClЎЎЎЎЎЎ BЈ®FЎў O ЎўS ЎЎЎЎCЈ®SЎў Cl ЎўOЎЎЎЎЎЎЎЎ DЈ®S ЎўO ЎўF
5ЎўПВБРОпЦКЦРјоРФЧоИхөДКЗЈә
AЈ®NaOHЎЎЎЎЎЎЎЎЎЎ BЈ®Al(OH)3 ЎЎЎЎЎЎCЈ®Mg(OH)2ЎЎЎЎ ЎЎDЈ®KOH
4ЎўПВБРұИҪПІ»ХэИ·өДКЗЈә
AЈ®ОИ¶ЁРФЈәH2O>H2SЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ BЈ®Сх»ҜРФЈәS>Se
CЈ®»№ФӯРФЈәH2S>H2SeЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ DЈ®ОўБЈ°лҫ¶ЈәS2->S
3ЎўјЧНйКЗТ»ЦЦёЯР§ЗеҪаөДРВДЬФҙЈ¬0.25molјЧНйНкИ«ИјЙХЙъіЙТәМ¬Л®Кұ·Еіц222.5kJИИБҝЈ¬ФтПВБРИИ»ҜС§·ҪіМКҪХэИ·өДКЗЈә
AЈ®2CH4(g)+4O2(g)==2CO2(g)+4H2O(l)Ј»ЎЎ ЎчH= +890kJЎӨmol-
BЈ®CH4(g)+2O2(g)==CO2(g)+2H2O(l)Ј»ЎЎЎЎ ЎчH= +890kJЎӨmol-
CЈ®CH4(g)+2O2(g)==CO2(g)+2H2O(l)Ј»ЎЎЎЎ ЎчH= Јӯ890kJЎӨmol-
DЈ®CH4(g)+2O2(g)==CO2(g)+2H2O(g )Ј»ЎчH= Јӯ890kJЎӨmol-
2ЎўПЦУРИзПВёчЧйОпЦК, ЖдЦР»ҜС§јьАаРНПаН¬, ҫ§МеАаРНТІПаН¬өДТ»ЧйКЗЈә
ЎЎЎЎЎЎ AЈ®SO2әНSiO2ЎЎЎЎ BЈ®CO2әНH2OЎЎЎЎ CЈ®HClәНNaClЎЎЎЎ DЈ®CCl4әНKCl
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com