
题目列表(包括答案和解析)
9.进行化学实验必须注意安全,下列说法不正确的是:
A. 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
B. 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂硼酸溶液
C. 配制硝酸硫酸的混合酸时,应将浓硝酸滴入中浓硫酸
D.不慎将浓硫酸沾到皮肤上,要立即用大量水冲洗,然后涂碳酸氢钠溶液
8.下列排列顺序正确的是:
A.微粒半径:Na+>K+>Cl->S2- B.稳定性:HI> HBr>HCl>HF
C.酸性: HClO4>H2SO4>H3PO4>H2SiO4 D.熔点: Al > Mg > Na > K
7.下列叙述正确的是:
A.元素的单质可由氧化或还原含该元素的化合物来制得
B.得电子越多的氧化剂,其氧化性就越强
C.阳离子只能得到电子被还原,只能作氧化剂
D.含有高价元素的化合物,一定具有强的氧化性
5.甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是
(CH3)2C==O+HCN→ (CH3)2C(OH)CN
(CH3)2C(OH)CN+CH3OH+H2SO4→CH2== C(CH3)COOCH3+NH4HSO4,
90年代新的反应是:CH3C≡CH+CO+CH3OH CH2==C(CH3)COOCH3,与旧法比较,新法的优点是:①原料无爆炸危险 ;②原料都是无毒物质;③没有副产物,原料利用率高;④对设备腐蚀性较小。
CH2==C(CH3)COOCH3,与旧法比较,新法的优点是:①原料无爆炸危险 ;②原料都是无毒物质;③没有副产物,原料利用率高;④对设备腐蚀性较小。
A. ①② B. ③④ C. ①③ D. ②④
6设NA为阿伏加德罗常数,下列说法不正确的是:
A.23gNa做还原剂可提供电子数为NA
B.在标准状况下,1mol戊烷的所含的原子数为17NA
C.常温常压下,22.4LNH3所含电子数目为10NA
D.常温常压下,1mol氩气含有原子数为NA
4.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是:
A. 利用电池外壳的金属材料
B. 回收其中的石墨电极
C. 防止电池中的汞、镉和铅等重金属离子对土壤和水的污染
D. 不使电池中渗泄的电解液腐蚀其它物品
3.在一定条件下, CO和CH4燃烧的热化学方程式分别为:
2CO(气) + O2(气) = 2CO2(气) ;△H=-566kJ
CH4(气) + 2O2(气) = CO2(气) + 2H2O(液) ;△H=-890kJ
现由1mol CO和3mol CH4组成的混合气, 在上述条件下完全燃烧时, 释放的热量为:
A.2912KJ B.2953KJ C.3236KJ D.3867KJ
2.1995年美国教授Lagow报道,他制得了碳的第四种同素异形体--链式炔碳:
… C--C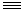 C--C
C--C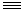 C …。该物质的一个分子中含300-500个碳原子,性质很活泼。据此判断链式炔碳的熔点,估计比石墨
A.高 B.低 C.相等 D.无法判断
C …。该物质的一个分子中含300-500个碳原子,性质很活泼。据此判断链式炔碳的熔点,估计比石墨
A.高 B.低 C.相等 D.无法判断
1.我国将全面禁止使用含铅汽油(含铅汽油中溶有能提高汽油抗震性能的四乙基铅),其主要目的是:
A.减少汽车尾气中氮氧化物的排放量 B.提高汽油的燃烧值
C.消除汽车尾气中的铅对大气的污染 D.使汽油燃烧得更充分
23、在20℃时氯化钠的溶解度为36.0g。现取一定量该温度下的饱和氯化钠溶液,用惰性电极电解。当阳极析出11.2L(标准状况)气体时,氯化钠完全消耗,所得溶液密度为1.20g/cm3。若忽略电极产生在溶液中的溶解,试计算:
(1)电解时所取饱和氯化钠溶液的质量。
(2)电解后溶液中氢氧化钠的物质的量浓度。
2007-2008学年度深圳宝安中学
新课标高一化学期末检测试卷
班级 姓名 学号 分数
22、有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
⑴元素名称: A __ ____ B ____ __ C ____ ___ D _ ______
⑵写出AB2 的电子式为: ______________
⑶画出D的原子结构示意图: ______ _____________,
用电子式表示化合物 C2D 的形成过程: _______ _____
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com