
题目列表(包括答案和解析)
23.(8分)(07全国改编)用A+、B-、C2-、D、E、F、和G分别表示含有18个电子八种微粒(离子或分子)。请回答:
⑴A元素是 、B元素是 、C元素是 (用元素符号表示)。
⑵D是由两种元素组成的双原子分子,其分子式是 。
⑶E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是 。
⑷F是由两种元素组成的三原子分子,其电子式是 。
⑸G是由两种元素组成,分子中含有4个原子,其分子式是 。
⑹A+、B-、C2-三种离子的半径从大到小的顺序为 。(用离子符号表示)
22.(7分))①②③④⑤五种元素,在元素周期表中的位置如图所示。回答下列问题:
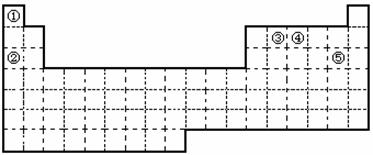
(1)上述五种元素中,金属性最强的元素在周期表中的位置是 ,该元素的单质在空气中燃烧的化学方程式为 。
(2)元素①和③可以形成众多的化合物,其中最简单的是(写化学式) ,该化合物中,化学键的类型为 (填“离子键”或“共价键”)。
(3)试写出元素④最高氧化物的水化物(浓溶液)与Cu反应的离子方程式:
,该反应中作氧化剂的是(写化学式) 。
(4)试用电子式表示元素⑤单质分子的形成过程 。
21.(6分) (07全国)现有五种离子化合物A、B、C、D和E,都是由下表中离子形成的:
|
阳离子 |
Ag+
Ba2+ Al3+ |
|
阴离子 |
OH-
Cl-
SO42- |
为鉴别它们,分别完成以下实验,其结果是:
a.B和D都不溶于水,也不溶于酸;
b.A溶于水后,与上述某阳离子反应可生成B,且A溶液与过量氨水反应生成白色沉淀
c.C溶于水后,与上述某阳离子反应可生成D,且C溶液与过量氨水反应生成白色沉淀
d.E溶于水后,与上述某阴离子反应可生成B;
e.A溶液与适量E溶液反应生成沉淀,再加过量E溶液,沉淀是减少,但不消失。
请根据上述实验结果,填空:
⑴写出化合物的化学式:A ,B ,
C ,D , E 。
⑵A溶液与过量E溶液反应后,最终得到的沉淀的化学式是 。
20.(8分)氯是一种海水富集元素。下图是一套制取并验证氯气部分化学性质的实验装置:

回答下列问题:
(1)装置I中,仪器a的名称为________________。
(2)当Cl2气流通过一段时间后,装置Ⅱ中溶液的pH值____7(填“>”“<”或“=”)
(3)当有少量Cl2气流通过后,装置Ⅲ中反应的离子方程式为_______________ 。
(4)当Cl2气流持续通过时,装置Ⅳ中干燥的有色布条能否褪色? 。
(5)装置V的作用是___________________________________________________。
19.(6分) 我国化工专家侯德榜发明的侯氏制碱法的化学原理是将二氧化碳通入氨水的氯化钠饱和溶液中,其化学反应方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
(1)在实验室中利用上述原理从反应所得混合体系中分离出碳酸氢钠晶体,应选用下列装置中的 ,(填写序号)该装置使用的玻璃仪器有
。


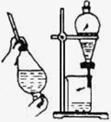
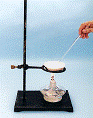
A B C D
(2)碳酸氢钠晶体受热易分解,写出其分解的化学方程式: 。
18.(07全国)已知氧化还原反应:
2 Cu(IO3)2+24 KI+12 H2SO4=2 CuI↓+13 I2+12 K2SO4+12 H2O
其中1 mol氧化剂在反应中得到的电子为
A.10 mol B.11 mol C.12 mol D.13 mol
 第Ⅱ卷(非选择题,共54分)
第Ⅱ卷(非选择题,共54分)
17.(07广东)下列关于元素周期表和元素周期律的说法错误的是
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,金属性逐渐增强,非金属性逐渐减弱
C.因为Na比K容易失去电子,所以Na比K的还原性强
D.O与S为同主族元素,且O比S的非金属性强
16.(07海南)下列实验现象的描述错误的是
A.氢气在氯气中燃烧生成绿色烟雾
B.红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒
C.点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰
D.钠在空气中燃烧,发出黄色的火焰,生成白色固体
15.(07上海)下列反应的离子方程式正确的是
A.氢氧化钠溶液中通入少量二氧化硫:SO2+OH-=HSO3-
B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.盐酸滴入氨水中:H++OH-=H2O
D.碳酸钙溶解于稀硝酸中:CO32-+2H+=CO2↑+H2O
14.(07江苏)下列有关实验的说法正确的是
A.除去铁粉中混有的少量铝粉.可加人过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.某溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com