
题目列表(包括答案和解析)
2.下列物质中既能导电,又属于强电解质的一组物质是( )
A.石墨、醋酸溶液、食盐晶体 B.熔融状态的KOH、熔融状态的NaCl
C.稀H2SO4、NaOH溶液、纯HNO3 D.液氨、石灰水、水银
1.下列叙述正确的是( )
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.元素由化合态转化为游离态,该元素一定被还原
C.非金属单质在氧化还原反应中一定做氧化剂
D.同一氧化还原反应中氧化剂发生还原反应,还原剂发生氧化反应
26.(9分)在标准状况下进行甲、乙、丙三组实验,三组各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量(mg) |
255 |
385 |
459 |
|
生成气体体积(mL) |
280 |
336 |
336 |
(1)甲组实验中,盐酸 ▲ (填“过量”“适量”或“不足量”),乙组实验中,盐酸 ▲ (填“过量”“适量”或“不足量”)。参考合适的数据计算出盐酸的物质的量浓度为 ▲ 。
(2)参考合适的数据组合求得的Mg、Al的物质的量之比为 ▲ 。
(3)在丙组实验之后,向容器中加入1 mol·L-1的氢氧化钠溶液,能使合金中的铝恰好溶解,不形成含铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶固体,求滤液中各溶质的物质的量和所加入氢氧化钠溶液的体积(写计算过程)。





高一化学第一学期期中考试试题
高一化学试题
25.(8分)根据信息试回答下列问题:
 信息1:H2O是一种极弱的电解质,其电离方程式为:H2O OH- + H+
信息1:H2O是一种极弱的电解质,其电离方程式为:H2O OH- + H+
而碳化钙(CaC2)与水反应可以看作是一种复分解反应:
CaC2 + 2H2O === Ca(OH)2 + C2 H2↑
信息2:已知固体甲、E、I、F均为常见的单质,其中E在常温下为气态。W是由两种常见元素组成,其与水的反应可类比碳化钙与水的反应。乙通常是一种红棕色粉末。G为白色胶状沉淀。W、G、H、I三种物质中都含有同一种常见金属元素。A沼气的主要成分,与氧气完全反应时的体积比是1∶2 。各物质有如下图所示的转化关系(部分反应的产物未全部表示)。


(1)I原子的结构示意图______▲________。
(2)按要求写方程式:
I → E的离子方程式:____________ _▲_________________
C → E的化学方程式:______________▲________________
(3)写出W和水反应的化学方程式_________________▲_________________
(4)取3mol F物质在一定条件下与足量水反应生成E,则此过程转移电子数目为__▲___
24.(8分)工业生产的纯碱中常含有少量的NaCl杂质。某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用下图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数。
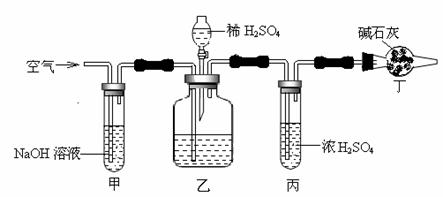
(1)甲装置的作用是 ▲ ;甲装置反应的离子方程式是 ▲ 。
(2)乙装置反应结束后,再通数分钟空气的作用是 ▲ 。
(3)若去掉丙装置,测得的CO2质量会 ▲ (填“偏大”、“偏小”或“无影响”)。
(4)若取ng样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为mg,实验结束后称得干燥管丁的总质量为w,则Na2CO3质量分数的计算式为 ▲ 。
(5)有同学认为在丁后面还要加一装置,请分析完成装置图于方框中。
23.(7分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

(1)试剂1是 ▲
(2)加入新制氯水后溶液中发生的离子反应方程式是 ▲ 、
▲ ;
(3)加入试剂2后溶液中颜色由淡黄色转变为淡红色的是因为 ▲ 。
(4)若向FeCl2溶液中加入NaOH溶液,可以发现生成沉淀,而且沉淀暴露在空气中将有颜色变化,此颜色变化为 ▲
22.(8分)下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500mL的操作,请按要求填空:
(1)所需浓H2SO4的体积为_____▲_____(用下一小题的仪器量取)。
(2)如果实验室有15mL、20mL、50mL量筒,应选用____▲___mL量筒最好。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌。
(4)将冷却至室温的上述溶液沿_____▲_____注入______▲______中,并用50mL蒸馏水洗涤烧杯2-3次,洗涤液要注入上述仪器中,并摇匀。
(5)加水至距刻度_____▲______时,改用胶头滴管加水,使溶液的凹液面正好跟刻度相平。
(6)误差分析:请用“偏高”“偏低”或“无影响”进行填空
① 定容时,观察液面俯视: ▲
② 摇匀后,液面低于刻度线,没有再加水: ▲
③ 取浓H2SO4时,倒出浓H2SO4后的量筒中还残留少量液体未处理: ▲
21.(6分)如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
 (1)图中有两处明显的错误是
(1)图中有两处明显的错误是
① ▲ ;
② ▲ 。
(2)A仪器的名称是 ▲ ,B仪器
的名称是 ▲ 。
(3)实验时A中除加入少量自来水外,还需要加
入少量的 ▲ ,其作用是 ▲ 。
20.(4分)(1)若向NaHSO4溶液中逐滴加入Ba(OH)2溶液,使原溶液中的SO42-恰好完全沉淀,试写出该反应的化学方程式 ▲
(2)明矾是一种无色晶体,可溶于水并形成Al(OH)3胶体来净水。已知明矾水溶液的主要成分是KAl(SO4)2 ,现向明矾溶液中逐滴加入Ba(OH) 溶液,当Al3+恰好全部沉淀时,试写出该反应的化学方程式
▲
溶液,当Al3+恰好全部沉淀时,试写出该反应的化学方程式
▲
19.(4分)在标准状况下,由CO和CO2组成的混合气体11.2 L,质量为18.8 g,则混合气体中 n(CO) :n(CO2)=____▲___;CO的物质的量的分数为_____▲_____;CO2的体积分数为___▲____;混合气体的的密度为____▲___ g/L。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com