
题目列表(包括答案和解析)
(二)量子力学的创始人:海森堡、薛定谔
玻尔、玻恩、狄拉克
1.量子力学是彻底的量子理论,是研究微观世界的基本理论工具。它不但能解释玻尔理论所能解释的现象,而且能够解释大量玻尔理论不能解释的现象,玻尔理论中的三点假设,在量子力学中也变成理论上推导出来的直接结果。
2.建立在量子力学基础上的原子理论与玻尔原子理论的区别:根据量子力学,核外电子的运动服从统计规律,而没有固定的轨道,我们只能知道它们在核外某处出现的几率大小,核外电子的这种运动情况可用“电子云”来形象描述,电子云稠密的地方就是电子出现几率大的地方。
(一)玻尔原子理论的困难:
具有两个以上电子的比较复杂的原子光谱,玻尔原子理论都遇到了不可克服的困难(在于理论内部的矛盾)。
玻尔理论是一种半经典的理论,一方面引入了量子假设,另一方面又应用经典理论计算电子轨道半径和能量。因此,玻尔理论在解释复杂的微观现象时遇到困难,乃是必然的。
(二)玻尔理论对氢光谱规律的解释:
En= E1 (巴耳末系)
E1 (巴耳末系)
h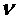 =E2-E1=
=E2-E1= E1-
E1-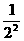 E1=-E1(
E1=-E1(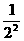 -
- )
)
又 ,则:
,则: =-E1(
=-E1(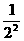 -
- )
)
 =-
=- (
(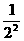 -
- )
)
计算:R=- =1.097373×107m-1,
=1.097373×107m-1,
也解释了帕邢系(红外区)(n=3)
预言了当时未发现的光谱系:(说明理论的正确)
赖曼系(紫外区)(n=1)
布喇开系(远红外区)(n=4)
注意:
1、氢光谱中的每个线系,都是原子从不同的高能级向某一低能级跃迁时发出的谱线。
2、光谱线上的每一条谱线都是大量处于同一能态的原子向同一低能级(态)跃迁的结果。
3、由于每个原子所处的能态不同,大量原子的跃迁在同一时刻,会发出不同频率的光束,因此光谱线上能够出现各种谱线。
(一)氢光谱的规律:1、氢光谱(可见光区)
每种元素都发出自己独特的光谱,各种元素的每条光谱线的频率都是固定不变的。
氢光谱在可见光区有四条谱线
红 Ha 0.6562mm
蓝 Hb 0.4861mm
紫 Hg 0.4340mm
紫 Hd 0.4101mm
2.巴耳末经验公式:(1885年瑞士中学教师)
(规律) =R(
=R(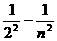 ), n=3, 4, 5
......
), n=3, 4, 5
......
式中R叫做里德伯恒量,测得R=1.096776×107m-1
计算与实验符合得很好,
此谱系称巴耳末系。
(三)氢原子的大小和能级:(玻尔理论对氢原子的应用)
1.能级:原子各个定态的能量值,叫做它的能级。
在正常情况下,原子处于最低能级,这时电子在离核最近的轨道上运动,这种定态叫做基态。
电子在离核较远的轨道上运动处于高能级状态,这种定态叫激发态。
2. 轨道半径公式(可能):rn=n2r1
轨道半径公式(可能):rn=n2r1
n=1, 2, 3 ......
En= E1
E1
式中r1代表第一条(即离核最近的一条)可能轨道的半径。
E1代表电子在第一条(即离核最近的一条)可能轨道的运动时的能量。n是量子数。
r1=0.53×10-10m
E1=-13.6ev,(E∞=0,电子的动能等于电势能绝对值的一半)
(二)玻尔原子理论的主要内容:
1.能级假设:原子只能处于一系列不连续的能量状态中,在这些状态中原子是稳定的,电子虽然做加速运动,但并不向外辐射能量,这些状态叫做定态。具有一定的能量,也叫能级。(能量指系统动能和势能的总和)
能级假设是针对原子的稳定性提出的,它承认核式模型,但假定原子只能处于一系列“不连续”的稳定状态中。
从宏观现象的“连续”的概念过渡到微观世界的“不连续”的概念,是人类对物质世界认识上的一次飞跃。
2.跃迁假设:原子从一种定态(设能量为E2)跃迁到另一种定态(设能量为E1)时,它辐射(或吸收)一定频率的光子,光子的能量由两种定态的能量差决定,即
h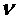 =E2-E1
=E2-E1
跃迁假设说明了原子发光的机制,这一条假设是针对原子发光的光谱是线状光谱提出的,运用了普朗克的量子理论。
3.轨道假设:原子的不同能量状态对应于电子的不同运行轨道,由于原子的能量状态是不连续的,因此电子的可能轨道也是不连续的,即电子不能在任意半径的轨道上运行,只有满足下列条件的轨道才是可能的:轨道半径r跟电子的动量mv的乘积等于h/2p的整数倍,即mvr=n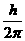 , n=1, 2, 3 ....,式中n是正整数叫量子数,这种现象叫做轨道的量子化。
, n=1, 2, 3 ....,式中n是正整数叫量子数,这种现象叫做轨道的量子化。
轨道量子化假设也是针对原子的核式模型提出的,是对第一条假设的补充。
(一)玻尔理论产生的背景:
1.背景:核式结构虽然能很好地解释a粒子散射实验,但跟经典的电磁理论发生了矛盾,这些矛盾说明从宏观现象总结出来的经典电磁理论不适用于微观现象。不解决这个矛盾,原子理论就不能前进,这就是产生玻尔原子理论的历史背景。
2.核式结构与经典电磁理论的矛盾:
①按经典电磁理论,电子在绕核作加速运动过程中,要向外辐射电磁波,因此能量要减少,电子轨道半径也要变小,最终会落到原子核上,因而原子是不稳定的;
②电子在转动过程中,随着转动半径的缩小,转动频率不断增大,辐射电磁波的频率不断变大,因而大量原子发光的光谱应该是连续光谱。
而事实上,原子是稳定的,原子光谱也不是连续的光谱,而是线状光谱。(明线光谱)
(三)卢瑟福原子核式结构模型:
在原子的中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电子在核外空间进而绕着核旋转。
(二)原子核的电荷和大小:
1.测知原子核的电荷:原子中的电子数等于原子序数。
2.意义:给元素排序提供了实验依据,元素的化学性质归根到底是由原子中的电子数决定的,从而是由原子核中的电荷数来决定的。
3.核的大小:直径10-14m以下
原子核的半径只相当于原子半径的万分之一,
原子核的体积只相当于原子体积的万亿分之一。
4.原子核密度很大,1立方厘米的原子核质量为107吨。
(一)原子核式结构的发现:
1.什么叫散射实验?
用各种粒子--x射线、电子和a粒子轰击很薄的物质层,通过观察这些粒子穿过物质层后的偏转情况,获得原子结构的信息,这种实验叫做散射实验。
2.为什么用a粒子的散射(实验)现象可以研究原子的结构?
原子的结构非常紧密,用一般的方法无法探测它内部的结构,要认识原子的结构,需要用高速粒子对它进行轰击。
①由于a粒子具有足够的能量可以接近原子的中心,
②a粒子可以使荧光物质发光,如果a粒子与其他粒子发生相互作用,改变了运动的方向,荧光屏便能够显示出它的方向变化。
3.a粒子散射装置
①放射源(Pa“坡”)玛丽·居里的祖国波兰。
②金箔:1mm,能透光,有3000多层原子厚。
 ③荧光屏 荧光屏和显微镜能够围绕金箔在一个
③荧光屏 荧光屏和显微镜能够围绕金箔在一个
④显微镜 圆周上转动,从而可以观察到穿过金箔后
⑤转动圆盘 偏转角度不同的a粒子
4.实验过程:实验室建在地下,通道大拐角(防光进入)
马斯登和盖革(卢瑟福的学生、助手)进入实验室后要静座半小时散瞳孔后进行观察(纯人工计数),这种观察是十分艰苦细致的工作,所用的时间也是相当长的。(1909年~~1911年两年的时间)。
5.实验结果:
①“绝在多数”(几十万个)a粒子穿过金箔后仍沿原来的方向前进
②“少数”(上万个)a粒子都发生了较大的偏转,
③并且“极少数”(1350角几十个,1800角十几个)a粒子的偏转超过了900,有的甚至几乎达到1800,象是被金箔弹了回来。
6.实验分析:马斯登和盖革把实验结果交给老师后,卢瑟福开始认为是实验错了(汤姆生是卢瑟福的老师,老师的观点能否轻易否定吗?)
根据原理论寻找新的解释,后来才发现应修改理论,三个多星期后,卢瑟福吹着口哨到了实验室,两个学生一听,老师已解决了这个问题。
①电子不可能使a粒子发生大角度散射,a粒子跟电子碰撞过程中,两者动量的变化相等,由于a粒子的质量是电子质量的7300倍,在碰撞前后,质量大的a粒子速度几乎不变,而质量小的电子速度要发生改变,因此,a粒子与电子正碰时,不会出现被反弹回来的现象。发生非对心碰撞时,a粒子也不会有大角度的偏转,可见,电子使a粒子在速度的大小和方向上的改变都是十分微小的。
②按照汤姆生的原子模型,正电荷在原子内部均匀地分布,a粒子穿过原子时,由于粒子两侧正电荷对它的斥力有相当大一部分互相抵消,使a粒子偏转的力也不会很大。a粒子的大角度散射现象,说明汤姆生模型不符合原子结构的实际情况。
③实验中发现极少数a粒子发生了大角度偏转,甚至反弹回来,表明这些a粒子在原子中的某个地方受到了质量、电量均比它本身大得多的物体的作用。
④金箔的厚度大约1mm,金原子的直径大约是3×10-10米,绝大多数a粒子在穿过金箔时,相当于穿过三千多个金原子的厚度,但它们的运动方向却没有发生明显的变化,这个现象表明了a粒子在穿过金箔时,基本上没有受到力的作用,说明原子中的绝大部分是空的,原子的质量和电量都集中在体积很小的核上。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com