
题目列表(包括答案和解析)
7、下列化合物中,既有离子键,又有共价键的是 ( )
A.CaCl2 B.HNO3 C.CO2 D.KOH
6、下列各组性质比较中,不正确的是( )
A、酸性:HClO4>HBrO4>HIO4 B、碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
C、氧化性:F2<Br2<I2 D、还原性:Li<Na<K
5、下列各图为元素周期表的一部分,表中的数字为原子序数,其中M的原子序数为37的是( )
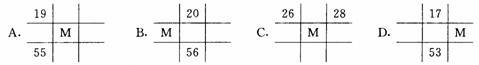
4.下列电子式书写正确的是
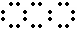
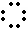
A. O C O B.Ca2+ [ Cl ]-2

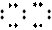
C.Cl C Cl D.Na+ [ O O ]2- Na+
3、甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是( )
A.x+16 B.x+4 C.x+8 D.x+18
2.元素的性质呈周期性变化的根本原因是( )
A.元素原子量的递增,量变引起质变
B.元素的原子半径呈周期性变化
C.元素原子的核外电子排布呈周期性变化
D.元素的金属性和非金属性呈周期性变化
1、以下互为同位素的是( )
A、石墨与金刚石 B、D2和T2
C、CO和CO2
D、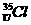 和
和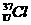
17.(12分)A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 ,乙物质的化学式是 •
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
。
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
。
(4)简述比较D与E金属性强弱的实验方法:
。
人教版必修2第一章《物质结构 元素周期律》测试题(A卷)
15. (15分)现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
(15分)现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
|
|
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
0.82 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
回答下列问题:
(1)③的元素符号是 ,⑧的元素名称是 。①在元素周期表中的位置是(周期、族) 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 ;名称是 ;碱性最强的化合物的电子式是: ;
属 化合物(填“离子”或“共价”)。
(3)比较④和⑦的氢化物的稳定性(用化学式表示) 。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
。
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:
。
|
(1)A、B、C、D、E的元素符号分别是:
A ,B ,C ,
D ,E
(2)A、B、C的的酸性由强到弱的顺序是(用化学式表示)
。
(3)A的最高价氧化物对应的水化物体现 (填“酸性 ”、“碱性”、“两性”),用离子方程式表示为:
。
(4)E为 (填“金属”、“非金属”),其单质可能为 (填“导体”、“非导体”、“半导体”),推断理由是
。
14.下列叙述正确的是
A.非金属原子间以共价键结合的物质都是共价化合物
B.含有共价键的化合物都是共价化合物
C.凡是能电离出离子的化合物都是离子化合物
D.凡是含有离子键的化合物都是离子化合物
高一 班 姓名 学号 成绩
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com