
题目列表(包括答案和解析)
20. 下列各组中化合物的性质比较,不正确的是
A.酸性:HClO4>HBrO4>HIO4 B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S> HCl D.还原性强弱: F- > Cl- > I-
19.第119号未知元素,有人称为“类钫”。根据周期表结构及元素性质变化趋势,有关“类钫”的预测的说法错误的是
A、单质有较高的熔点 B、“类钫”在化合物中呈+1价
C、“类钫”具有放射性 D、“类钫”单质与水剧烈反应
18.无机化学命名委员会(国际组织)在1989年作出决定:把周期表原先的主、副族号取消,由左到右按原顺序编为18列,如碱金属为第1列,稀有气体为第18列。按这个规定,下列说法正确的是
A第3列元素种类最多,第14列的化合物种类最多 B.每1列都有非金属元素
C.从上到下第1列元素的单质熔点逐渐升高,而第17列元素的单质熔点逐渐降低
D.只有第2列元素的原子最外层有2个电子
17.在下面元素周期表中画出金属元素与非金属元素的分界线:
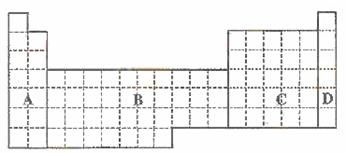
16.主族元素的最高正价= = = ( 、 除外);非金属元素最低负价= 。以R代表第ⅣA、ⅤA、ⅥA、ⅦA族的非金属元素,写出它们的气态氢化物的通式: 、 、 、 ;写出它们的最高价氧化物的通式: 、 、 、 ;写出它们的最高价氧化物的水化物通式: 、 、 、 。以R代表第ⅠA、ⅡA、ⅢA族的金属元素,写出它们的最高价氧化物的通式: 、 、 ;写出它们的最高价氧化物的水化物通式: 、 、 。
15.同一周期,从左到右,原子半径逐渐 ,原子核对最外层电子的引力逐渐 ,
金属性逐渐 ,非金属性逐渐 ;同一主族,从上到下,原子半径逐渐 ,原子核对最外层电子的引力逐渐 ,金属性逐渐 ,非金属性逐渐 .
14.元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化 B.元素原子量依次递增
C.元素原子最外层电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化
13.请写出所有主族元素和稀有气体的元素符号、名称和原子序数:
|
|
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
12.不查元素周期表,请指出35和116号元素在周期表中的位置: 、
。
11.元素周期表中有 个纵行 个族,包括 个主族 个副族,还有 族和 族。主族序数= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com