
题目列表(包括答案和解析)
20.(14分)实验室用密度为1.18 g/mL,质量分数为36.5%的浓盐酸配制250 mL 0.1 mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250 mL 0.1mol/L的盐酸溶液
|
应量取浓盐酸体积/mL |
应选用容量瓶的规格/mL |
除容量瓶外还需要的其它仪器 |
|
|
|
|
(2)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)
___ ___ _;
A.用30 mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡;
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀;
C.将已恢复到室温的盐酸沿玻璃棒注入250mL的容量瓶中;
D.将容量瓶盖紧,振荡,摇匀;
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切;
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处;
(3)操作A中,将洗涤液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢复到室温,这是因为 ;
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作 ;若加蒸馏水时不慎超过了刻度线 ;若定容时俯视刻度线___________________。
(5)若实验过程中出现如下情况如何处理?
a.加蒸馏水时不慎超过了刻度线 ;
b.向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面 。
19.(6分)就有关物质的分离回答下面的问题:
(1)分离沸点不同但又互溶的液体混合物,常用什么方法?试举例说明。
答: ;
(2)在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。
答: 。
18.质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,无固体析出,所得到的溶液密度为q g/mL ,物质的量浓度为c。则溶液中溶质的相对分子质量为
A.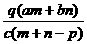 B.
B.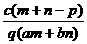
C.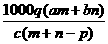 D.
D.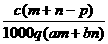
高一化学第一次阶段性测试试题
高 一 化 学
命题人:周国军 审核:高一化学备课组
第Ⅱ卷(非选择题,共56分)
17.配制一定物质的量浓度的下列溶液时,造成实验结果偏高的是
A.配制100 mL 1.00mol/L的NaOH溶液时,发现NaOH已经潮解,仍继续称量
B.配制100 mL 1.00mol/L的NaCl溶液时定容时俯视液面
C.配制50 mL 2.00mol/L的Na2CO3溶液时,被称量物与砝码位置放反称量
D.配制80 mL 0.10mol/L的CuSO4溶液时,准确称取2.0 g胆矾晶体,用100 mL 容量瓶进行准确配制
16.设NA代表阿伏加德罗常数的值,下列说法正确的是
A.2.4 g金属镁在反应中全部变成镁离子时,失去的电子数目为0.1NA
B.17 g NH3所含的电子数目为10NA
C.28g C2H4气体中所含的氢原子数目为NA
D.58.5 g NaCl中所含有的Na+离子数目为NA
15.下列各物质所含原子数目,按由大到小顺序排列的是
① 0.5mol NH3 ② 标准状况下22.4 L He ③ 4℃ 9mL 水 ④0.2mol H3PO4
A.①④③② B.④③②①
C.②③④① D.①④②③
14.与50 mL 0.1 mol·L-1 Na2CO3 溶液中Na+的物质的量浓度相同的溶液是
A.25 mL 0.2mol·L-1的 Na2SO4溶液 B.100 mL 0.2mol·L-1的NaCl溶液
C.25 mL 0.2mol·L-1 的NaCl溶液 D.10 mL 0.5mol·L-1的Na2CO3溶液
13.某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,不减少,则该溶液中
A.一定有SO42- B.可能有SO42-或Ag+
C.一定无Ag+ D.还可能有CO32-
12.将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中不正确的是
A.该分散系不能发生丁达尔现象 B.该分散质颗粒能透过滤纸
C.该分散质颗粒能透过半透膜 D.该分散质颗粒能发生布朗运动
纳米科技是21世纪经济发展的发动机。人们会利用纳米级(1-100 nm,1nm =10-9m )微粒物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用。请解答11、12两题。
11.下列分散系与纳米级微粒在直径上具有相同数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com