
题目列表(包括答案和解析)
17、本题共3小题(共10分)
(1)写出下列物质在水溶液中的电离方程式
氯化铜
硫酸铝
(2)写出下列反应的离子方程式
锌和稀硫酸反应
碳酸钙与稀盐酸混合
(3)标出下列反应的电子转移的方向和数目:
MnO2 + 4HCl(浓) === MnCl2 + Cl2 ↑ + 2H2O
16、本题共2小题(共10分)
(1)等质量的CO和CO2,物质的量之比为 ;
氧原子个数之比为
同温同压下,CO和CO2的密度之比为 。
(2)200mL 1mol/L Al2(SO4)3溶液和100mL 2mol/LAl2(SO4)3溶液所含SO42-离子浓度之比为 ,SO42-离子数目之比为 。
15、本题共2小题,(共8分)
(1)下列关于容量瓶及其使用方法的叙述,正确的是 (填序号,多选倒扣分)
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④可用容量瓶贮存配制好的溶液
⑤可以用500mL容量瓶配制480mL溶液
6容量瓶上标有温度和容积
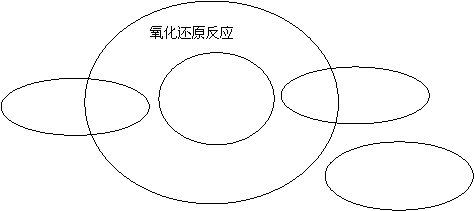
(2)下图表示分解、化合、置换、复分解四种反应类型和氧化还原反应的关系,请它们的对应关系填入下图中:

14、 若以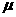 表示CO2的摩尔质量,v表示在标准状态下CO2的摩尔体积,ρ为在标准状态下CO2的密度,NA为阿伏加德罗常数,m、△分别表示每个二氧化碳分子的质量和体积,下面是四个关系式
表示CO2的摩尔质量,v表示在标准状态下CO2的摩尔体积,ρ为在标准状态下CO2的密度,NA为阿伏加德罗常数,m、△分别表示每个二氧化碳分子的质量和体积,下面是四个关系式
① ②
②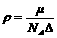 ③
③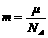 ④
④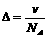 其中
其中
A.①和②都是正确的 B.①和③都是正确的
C.②和④都是正确的 D.①和④都是正确的
高一年级化学第一学期期中考试试卷
化 学
第Ⅰ卷 选择题答案(共50分)
第II卷 非选择题(共50分)
13、配制500mL1.0mol/L的NaCl溶液时,下列操作会使实际浓度偏高,偏低还是不变的判断中正确的是:
A、摇匀后,液面低于刻度线,没有再加水; 偏低
B、移液过程中,不小心溅出少量溶液; 偏低
C、配制用的NaCl固体不纯净; 不变
D、定容时,俯视刻度线; 偏高
12、为除去粗盐中的Ca 2+、Mg 2+、SO4 2-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液 正确的操作顺序是
A、①④②⑤③ B、④①②⑤③
C、②⑤④①③ D、⑤②④①③
11、等体积的空气和二氧化碳混和,并使之在高温下跟足量的焦炭反应,若氧气和二氧化碳最后全部转化成一氧化碳,则反应后的气体中一氧化碳的体积分数约是
A.0.60 B.0.64 C.0.70 D.0.75
10、氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
 Al2O3
+ N2 + 3C
2AlN + 3CO
Al2O3
+ N2 + 3C
2AlN + 3CO
下列有关该反应的叙述不正确的是
A.氮化铝中氮元素的化合价为-3
B.上述反应中,电子转移的数目为6mol
C.在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂
D.该反应不属于四种基本反应类型中任一种
9、下列叙述正确的是
A.化合反应一定是氧化还原反应
B.凡是两种或两种以上的物质发生的反应就属于化合反应
C.物质只有和氧气发生化合反应才是氧化反应
D.镁条在空气中燃烧既属于化合反应又属于氧化还原反应
8、设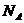 为阿伏加德罗常数,下列说法中正确的是( )
为阿伏加德罗常数,下列说法中正确的是( )
A.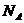 个氢气分子所占的体积为22.4L
个氢气分子所占的体积为22.4L
B.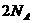 个二氧化碳分子的质量为88g
个二氧化碳分子的质量为88g
C.0.1mol/L 的NaCl溶液中,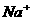 与
与 离子总数为
离子总数为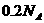
D.17g NH3中所含原子数为4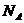
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com