
题目列表(包括答案和解析)
20.(7分)化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
⑴ 硅是无机非金属材料的主角。请你举出两种含硅的材料名称 、 。
⑵ 大量使用化石燃料的最直接的危害是造成大气污染,如“温室效应”、“酸雨”等都与大量使用化石燃料有关。请你举出两种防治酸雨的措施 、 。
⑶实验室有三瓶失去标签的无色溶液:氯化钾、氢氧化钙和稀硫酸,可用一种试剂一次鉴别它们。甲同学选的是一种正盐溶液,乙同学选的是一种有色试剂,他们都得到了正确结论。试推断甲、乙两位同学选用的试剂:
甲 __________ ,乙 _________ 。还可以用__________。(均填名称)
19.(7分)A-L所代表的各物质是中学化学里常见的物质,已知B、J是单质,A是化合物,E的溶液遇到KSCN溶液变成红色。A-L各物质之间相互反转化的关系如图所示(未注明必要的反应条件)。请回答:
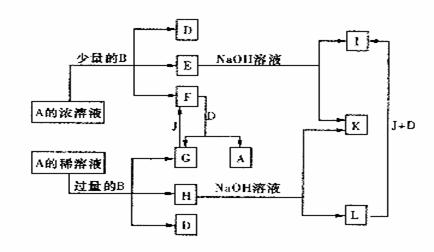
(1)B和A的浓溶液反应的条件是________,而常温下反应难以进行的原因是 ________________________________________________。
(2)写出F和G相互转化的化学方程式:
F→G:_______________________;G→F:______________________。
(3)写出E→I 的离子方程式:_____________________________________。
(4)L转化成 I 的现象是____________________________,有关反应的化学方程式为 ___________________________。
18、(15分)某研究性学习小组的同学对Cl2使有色物质褪色的机理进行了探究。
甲同学设计了如下图所示的实验装置并进行实验:


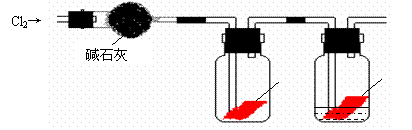
⑴ 甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因 ;
⑵ 甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象。你认为他预期的实验现象是 ,由此得出Cl2使有色物质褪色的机理是 。
⑶ 乙同学认为甲设计的实验装置即使改进后还缺少一部分。请你将乙认为缺少的部分在上图中的相应位置画出,并在添加的装置中标明需要放入的最合适的化学试剂的名称。
⑷ 请你写出Cl2和“③”中“最合适的化学试剂”反应的离子方程式 。
17、(9分)实验室需配制4.6 mol·L-1的H2SO4溶液0.5 L。
⑴ 需要浓度为18.4 mol·L-1的浓硫酸 mL;
⑵ 需要用的玻璃仪器除玻璃棒、量筒外还有 ;
⑶ 配制过程中下列操作导致溶液浓度偏高的是 。
(A)移液时未充分洗涤烧杯和玻棒
( B)移液时未用玻棒引流而使少量液体外溢
(C)定容俯视刻度线
16.下列离子在溶液中因发生氧化还原反应而不能大量共存的是 ( )
A.H3O+、NO3-、Fe2+、Na+ B.Ag+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42- D.Cu2+、NH4+、Br-、OH-
第II卷(非选择题 共52分)
15.下列叙述正确的是
A.常温常压下,5.6 L NH3的物质的量为0.25 mol
B.0.5 mol H2的质量为1 g,体积为11.2 L
C.40 g NaOH溶于1 L水中,得到的溶液物质的量浓度为l mol·L-1
D.9 g H2O中氧原子数与8 g O2中氧原子数相等
14.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
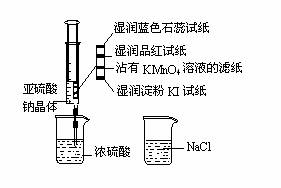 A.蓝色石蕊试纸先变红后褪色
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有KMnO4溶液
滤纸均褪色证明了SO2漂白性
C.湿润淀粉KI试纸未变蓝说明
SO2的氧化性弱于I 2
D.NaCl溶液可用于除去实验中
多余的SO2
13、高铁酸钾 (K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要反应方程为:2Fe(OH)3 +3ClO -+4OH- =2FeO42- +3Cl- +5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
下列有关说法不正确的是:
A. 高铁酸钾中铁显+6价
B. 湿法中每生成1mol Na2FeO4 转移3mol电子
C.干法中每生成1mol Na2FeO4 转移4mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质
12、若NA表示阿佛加德罗常数,下列说法正确的是( )
(A)1 mol Cl2作为氧化剂得到的电子数为NA
(B)在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子
(C)14 g氮气中含有7NA个电子
(D)NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4
11、向两烧杯中分别加入等足量的铝分别与等物质的量浓度的稀硫酸和氢氧化钠溶液反应,放出的气体体积在标准状况下相等,则所取稀硫酸和氢氧化钠溶液的体积比为
A 1︰2 B 3︰2 C 3︰1 D 6︰1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com