
题目列表(包括答案和解析)
9、在一定温度下,可逆反应A(g)+3B(g)
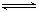 2C(g)达到平衡状态的标志是
2C(g)达到平衡状态的标志是
A. C生成的速率与A分解的速率2倍相等
B. 单位时间生成n mol A,同时生成3n mol B
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1∶3∶2
7、已知反应X+Y= M+N为吸热反应,对这个反应的下列说法中正确的是
A、X的能量一定低于M的,Y的能量一定低于N的
B、因为该反应为吸热反应,故一定要加热反应才能进行
C、破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D、X和Y的总能量一定低于M和N的总能量

|
A、NiO(OH) B、Ni(OH) 2 C、H2 D、H2和NiO(OH)
6、下列说法中正确的是
A、镍氢电池、锂离子电池和碱性锌锰干电池都是二次电池
B、燃料电池是一种高效但是会污染环境的新型电池
C、化学电池的反应基础是氧化还原反应
D、铅蓄电池放电的时候正极是Pb负极是PbO2
5、反应A+3B=4C+2D,在不同条件下反应,其平均反应速率v(X)(表示反应物的消耗速率或生成物的生成速率)如下,其中反应速率最快的是
A.v(A)=0.4mol/(L·s) B.v(B)=0.8mol/(L·s) C.v(C)=1.2mol/(L·s) D.v(D)=0.7mol/(L·s)
4、.某原电池的离子方程式是 Zn + Cu2+ = Zn2+ + Cu,该原电池正确的组成是
|
|
正极 |
负极 |
电解质溶液 |
|
A. |
Cu |
Zn |
HCl |
|
B. |
Zn |
Cu |
CuSO4 |
|
C. |
Cu |
Zn |
CuSO4 |
|
D. |
Cu |
Zn |
ZnCl2 |
3、下列说法中错误的是
A、化学反应中的能量变化通常表现为热量的变化
B、化学键的断裂和形成是化学反应中能量变化的主要原因
C、需要加热才能发生的反应一定是吸热反应
D、反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
2、.下列化合物中既有离子键又有共价键的是
A.KBr B.NaOH C.HBr D.N2
1、对发现元素周期律贡献最大的化学家是
A、牛顿 B、道尔顿
C、阿佛加德罗 D、门捷列夫
22、.⑴(5分)在下列事实中,什么因素影响了化学反应的速率?
①夏天的食品容易霉变,冬天就不容易发生该现象 ;
②熔化的氯酸钾放出气泡很慢,撒入少量二氧化锰很快产生气体 ;
③工业上常将固体燃料粉碎,以提高燃烧效率 ;
④同浓度的硫酸和盐酸与大小且质量相同的锌粒反应,产生气体硫酸快、盐酸慢 ;
⑤集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸 。
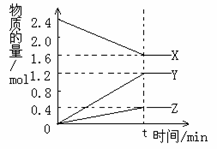 ⑵(8分)在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如右图。反应在t时到达平衡,依图所示:
⑵(8分)在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如右图。反应在t时到达平衡,依图所示:
①该反应的化学方程式是 。
②反应起始至t,Y的平均反应速率是 。
③X的物质的转化率是__________________。
④关于该反应的说法正确的是_________
A.到达t时刻该反应已停止;
B.在t时刻之前X的消耗速率大于它的生成速率;
C.在t时刻正反应速率等于逆反应速率;
D.在t时刻达到平衡是因为此时反应物总物质的量与生成物总物质的量相等。
20、(11分)
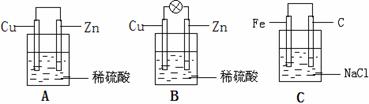
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察锌片上有气泡,再平行插入一块铜片,可观察到铜片 (填“有”或“没有”)气泡产生。再用导线把锌片和铜片连接起来(见下图A),组成一个原电池,负极为 ,正极的电极反应式为 ;
(2)如果烧杯中最初装入的是2mol/L 500mL的稀硫酸溶液,构成铜锌原电池(见下图B,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中硫酸的物质的量浓度为(溶液体积变化忽略不计) _________ ;
(3)金属的腐蚀分为两种:化学腐蚀(与化学物质直接接触而发生化学反应)和电化学腐蚀(由于构成原电池而发生电极反应),把铁片和石墨棒用导线相连插入氯化钠溶液中(见下图C),放置数天后,主要发生 腐蚀,写出有关反应式 __________________________________________________________ ;(化学腐蚀写化学方程式,电化学腐蚀写电极反应式)
(4)生活中利用原电池原理生产了各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其主要原因是 。
A、回收利用电池外壳的金属
B、防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
 C、防止电池中渗泄的电解液腐蚀其他物品
C、防止电池中渗泄的电解液腐蚀其他物品
D、回收其中石墨电极
21(12分).⑴笑气(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为 ,由此可知它 (填“含有”或“不含”)非极性键。
⑵、在NaCl、NaOH、N2、H2S中,
只含有离子键的是 ,只含有极性键的是 ,
只含有非极性键的是 ,既含有离子键又有极性键的是 。
⑶、下列各题中有关物质的比较,请用“>”、“<”、“=”填空:
①熔沸点: F2 Cl2 HF HCl;
②氧化性: F2 S, N2 O2;
③热稳定性:CH4 NH3, HCl HI。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com