
题目列表(包括答案和解析)
28. (10分,要求写出规范的解题过程)
(1)36.5%的浓盐酸,密度为1.19
g·cm-3,求其物质的量浓度?(列出计算式)
(2)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:
MnO2+4HCl(浓) MnCl2+
Cl2+2H2O。
若产生的氯气在标况下的体积为11.2L,试计算:
①参加反应的MnO2的质量。
②参加反应的HCl的物质的量。
MnCl2+
Cl2+2H2O。
若产生的氯气在标况下的体积为11.2L,试计算:
①参加反应的MnO2的质量。
②参加反应的HCl的物质的量。
27. (10分)(1)含有9 NA个电子的 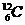 质量为
kg,其中含有
mol质子;
个中子。
(2)标准状况下448mL某气体的质量为1.28g,该气体的摩尔质量约为
。
(3)1.0L含9.03×1023个Cl-的AlCl3溶液的物质的量浓度为
。
(4)同温、同压下,某瓶充满O2时质量为116g,充满CO2时质量为122g,充满A时为114g,则A的相对分子质量为 。
质量为
kg,其中含有
mol质子;
个中子。
(2)标准状况下448mL某气体的质量为1.28g,该气体的摩尔质量约为
。
(3)1.0L含9.03×1023个Cl-的AlCl3溶液的物质的量浓度为
。
(4)同温、同压下,某瓶充满O2时质量为116g,充满CO2时质量为122g,充满A时为114g,则A的相对分子质量为 。
26. (8分)某学生用溶质质量分数为98%、密度为1.84 g·cm-3的浓硫酸,配制0.3mol/L的硫酸溶液500mL。试回答下列问题: (1)计算所需浓硫酸的体积 (计算结果保留到小数点后1位)。 (2)从下列用品中选出该实验一定要用的仪器 (填序号)。 A.1000mL烧杯 B.250mL烧杯 C.漏斗 D.10mL量筒 E.100mL量筒 F.500mL容量瓶 G.1000mL容量瓶 H.500mL烧瓶 I.托盘天平 除选用上述仪器外,尚缺少的必要仪器或用品是 。 (3)该学生根据计算结果,进行如下实验操作: ①用量筒量取计算所需体积的浓硫酸; ②向量筒中加入少量蒸馏水,并用玻璃棒搅拌; ③立即将稀释后的溶液转入容量瓶中; ④然后将蒸馏水注入容量瓶直至刻度线; ⑤把容量瓶盖盖紧,再振荡摇匀; ⑥定容摇匀后液面下降又补加水。 你认为上述实验操作中正确的是 (用编号表示)。
25.  (5分)
(5分) 下列反应中,不是氧化还原反应的是 ;属于氧化还原反应的,请找出在反应中化合价发生变化的元素,并将其反应前后的化合价标在元素符号的正上方
+7 -2
+6 +4 0
例:2KMnO4 K2MnO4+ MnO2+O2↑
①2FeCl2+Cl2
下列反应中,不是氧化还原反应的是 ;属于氧化还原反应的,请找出在反应中化合价发生变化的元素,并将其反应前后的化合价标在元素符号的正上方
+7 -2
+6 +4 0
例:2KMnO4 K2MnO4+ MnO2+O2↑
①2FeCl2+Cl2 2FeCl3
②Na2CO3+2HCl 2NaCl+H2O+CO2↑
③C+H2O CO+H2
④CuO+2HNO3
CO+H2
④CuO+2HNO3 Cu(NO3)2+H2O
⑤MnO2+4HCl(浓) MnCl2+
Cl2↑+2H2O
24. 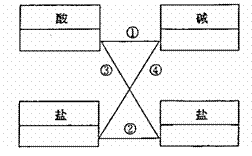 (8分)从稀盐酸、稀硫酸、石灰水、烧碱溶液、氢氧化钡溶液、氯化钠溶液、纯碱溶液、氯化钡溶液八种物质中,选出四种物质,使得图示中各线条相连的物质均能反应生成沉淀。将选出物质的化学式填写在图示相应的方框里,并写出③、④两步反应的化学方程式。
③
;
④
。
(8分)从稀盐酸、稀硫酸、石灰水、烧碱溶液、氢氧化钡溶液、氯化钠溶液、纯碱溶液、氯化钡溶液八种物质中,选出四种物质,使得图示中各线条相连的物质均能反应生成沉淀。将选出物质的化学式填写在图示相应的方框里,并写出③、④两步反应的化学方程式。
③
;
④
。
23. (6分)写出下列物质的电离方程式: (1)HNO3 。 (2)Ba(OH)2 。 (3)NaHSO4 。 (4)(NH4)3PO4 。 (5)K2CO3 。 (6)Fe2(SO4)3 。
22.  (9分)有A、B、C、D四种物质,它们可能是四氧化三铁、稀硫酸、硫酸铜溶液和水等物质中的一种。另有甲、乙、丙、丁四种气体,它们可能是二氧化碳、氧气、氢气和一氧化碳等四种气体中的一种,其中丁气体能使澄清的石灰水变浑浊。各气体与物质间有如下所示的反应和变化关系:
①铁 + 甲(气) B(黑色固体)
②铁 + C 硫酸亚铁 + 乙(气)
③乙(气)+ 甲(气) A
④丙(气)+ 甲(气) 丁(气)
⑤B + 丙(气) 铁 + 丁(气)
⑥铁 + D 硫酸亚铁 + 铜
(9分)有A、B、C、D四种物质,它们可能是四氧化三铁、稀硫酸、硫酸铜溶液和水等物质中的一种。另有甲、乙、丙、丁四种气体,它们可能是二氧化碳、氧气、氢气和一氧化碳等四种气体中的一种,其中丁气体能使澄清的石灰水变浑浊。各气体与物质间有如下所示的反应和变化关系:
①铁 + 甲(气) B(黑色固体)
②铁 + C 硫酸亚铁 + 乙(气)
③乙(气)+ 甲(气) A
④丙(气)+ 甲(气) 丁(气)
⑤B + 丙(气) 铁 + 丁(气)
⑥铁 + D 硫酸亚铁 + 铜
(1)试推断A、B、C、D和甲、乙、丙、丁各是何物质,写出指定物质的化学式。A: C: D: ;甲: 乙: 。 (2)写出反应⑤的化学方程式: 。 (3)上述反应中属于置换反应的是 。
21. (4分)下列各组物质中均有一种物质的类别与其它3种不同 A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、HNO3 则这4种物质依次是(填化学式): A ;B ;C ;D 。
20. 配制一定物质的量浓度的NaOH溶液时,造成最终浓度偏低的原因可能是 ①称量时已观察到NaOH吸水 ②容量瓶事先未烘干 ③移液时有少量液体流出 ④未洗净烧杯或玻璃棒 ⑤未恢复到室温即转移定容 ⑥定容时观察刻度线俯视 ⑦定容摇匀后液面恰好与刻度线相切 ⑧转移溶液时玻璃棒靠在刻度线上方 A.①②③④ B.①③④⑦⑧ C.①③⑤⑦ D.①②④⑥⑧
第Ⅱ卷 (非选择题 共60分)
19. 配制一定物质的量浓度的氯化钠溶液时,出现下列情况,肯定不必重新配制的是 A.转移溶液时不慎溅出数滴 B.加蒸馏水时不慎溅出数滴 C.加蒸馏水时不慎超过了刻度线 D.摇匀时有少量液体流出
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com