
题目列表(包括答案和解析)
22.有一表面被氧化成氧化钠的金属样品5.22g,投入到100g水中,产生气体2.24L(标况)。求:
⑴、此样品中单质钠的物质的量?
21.某温度下,一定量的某Na2SO3溶液的溶质质量分数为20%,在该溶液中加入1g Na2SO3·7H2O晶体后成为饱和溶液,此时溶液的体积为15.0mL,溶质质量分数为22%。试求:
(1)该温度下亚硫酸钠的溶解度。
(2)此时亚硫酸钠的物质的量浓度。
20.(本题10分)世界环保联盟即将全面禁止在自来水中加氯气(Cl2,黄绿色气体),推广采用光谱高效消毒剂二氧化氯,目前欧州和我国主采用Kesting法[原料为氯酸钠(NaClO3)与盐酸]制取ClO2,该法的缺点是同时会产生Cl2。该法制ClO2的化学方程式为
2NaClO3+4HCl == 2ClO2↑+Cl2↑+2NaCl+2H2O
(1)若生成0.1mol Cl2,转移的电子的物质的量为 ,该反应中氧化产物为 。
(2)在题中化学方程式中标出电子的转移的方向和数目。
(2)盐酸在反应中显示出来的性质是:(填写编号) 。两者的物质的量之比 。
①具有还原性和不稳定性 ② 具有酸性和氧化性 ③有氧化性和不稳定性 ④具有酸性与还原性
19.(本题8分)化学中有许多概念是相对的,又是统一的。右图反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
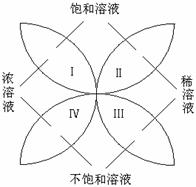 (1)从右图可以看出,饱和溶液与浓溶液、稀溶液的关系是
。
(1)从右图可以看出,饱和溶液与浓溶液、稀溶液的关系是
。
(2)0.9%的医用生理盐水可归于右图中 区域(选填"Ⅰ"、"Ⅱ"、"Ⅲ"或"Ⅳ");现有一瓶接近饱和的NaCl溶液,若要使它变为饱和溶液,一般采用的方法是
或 。
(3)生产上要配制6L1mol/L的盐酸来清洗钢材,需36.5%的盐酸(密度为1.2g/cm3)__________mL。
18.(本题6分)配制100 mL 1.10mol·L-1NaOH溶液时,某学生操作如下:将准确称量的4.4 g NaOH固体放入烧杯中,加入约30 mL蒸馏水,用玻璃棒搅拌使其溶解后,立即将烧杯中溶液注入100 mL容量瓶中,然后往容量瓶中小心加蒸馏水,直到液面接近刻度1cm ~ 2cm处,改用胶头滴管加蒸馏水,使溶液凹液面的最低点恰好与刻度线相切,再把容量瓶塞子塞紧,振荡摇匀。
(1)该生操作中的错误有:
。
(2)该学生称量4.4 g NaOH时不小心是将NaOH放在右盘,砝码放在左盘(1g以下用游码)进行的,这项操作将导致实际称得的NaOH固体质量 (填"偏大"、"偏小"或"无影响"),最后所配溶液的物质的量浓度是 mol·L-1。
17.(本题6分)含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:镁铝合金 溶液
溶液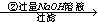 得到沉淀的质量为m2g;
得到沉淀的质量为m2g;
实验设计2:镁铝合金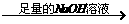 生成的气体在标准状况下的体积为V1L。
生成的气体在标准状况下的体积为V1L。
请回答以下问题:
(1)写出实验设计1中单质铝发生反应的第①步离子方程式:________________________________
(2)写出实验设计2中反应的离子方程式:________________________________________________
16.设N为阿伏加德罗常数值,若a g某气体中含有分子数b,则c g该气体在标准状况下的体积是
A.22.4ab/cN L B.22.4ac/bN L C.22.4b/acN L D.22.4bc/aN L
 选择题答案填写表格:
选择题答案填写表格:
15.物质的量浓度相同的NaCl、MgCl2、FeCl3溶液,分别与等体积等物质的量浓度的AgNO3溶液完全反应,所用去三种溶液的体积比为
A. 6:3:2 B. 1:2:3 C. 3:2:1 D. 1/3:1/2:1
14.根据世界环保联盟的要求,广谱消毒剂ClO2将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,反应后Na2SO3转化为Na2SO4,则反应物NaClO3和Na2SO3的物质的量之比为
A.1∶1 B.1∶2 C.2∶1 D.3∶1
13.人体正常的血红蛋白中含有Fe2+,若误服NaNO2,则导致血红蛋白中Fe2+转变为高铁血红蛋白而中毒。服用维生素C可解除NaNO2中毒。下列有关叙述正确的是
A. NaNO2是还原剂 B. 维生素 C是氧化剂
C. 维生素C将NaNO2还原 D. 维生素C被氧化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com