
题目列表(包括答案和解析)
2.
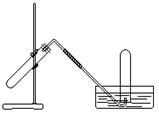 右图装置可用于
(A)加热NaHCO3制CO2
(B)用Cu与稀HNO3反应制NO
(C)用NH4Cl与浓NaOH溶液反应制NH3
(D)用NaCl与浓H2SO4反应制HCl
右图装置可用于
(A)加热NaHCO3制CO2
(B)用Cu与稀HNO3反应制NO
(C)用NH4Cl与浓NaOH溶液反应制NH3
(D)用NaCl与浓H2SO4反应制HCl
<div align="center">
1.
2.有离子参加或生成的反应叫做离子反应,电解质在水溶液中的反应属于离子反应,离子反应可用离子方程式表示。离子方程式是用实际参加反应的离子的符号表示离子反应的式子。它表示同一类型的所有的离子反应。如Ca2++CO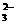
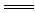 CaCO3↓表示可溶性钙盐和可溶性碳酸盐在溶液中进行的反应。书写离子方程式可按以下步骤:
CaCO3↓表示可溶性钙盐和可溶性碳酸盐在溶液中进行的反应。书写离子方程式可按以下步骤:
①写:写出化学方程式,并配平;
②拆:将可溶性强电解质写成离子形式,难溶、难电离的物质、氧化物和气体写成化学式;
③删:删去两边没反应的离子;
④查:检查是否符合质量守恒、电荷守恒、反应事实等。
如何判断一个离子方程式的正误呢?一个正确书写的离子方程式,应当是:
①必须符合客观事实。如离子方程式Cu+2H+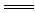 Cu2++H2↑很显然是错误的。
Cu2++H2↑很显然是错误的。
②必须符合拆写原则。如将石灰石加入稀盐酸中的离子方程式写成CO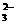 +2H+
+2H+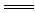 H2O+CO2↑就是错的。错在将难溶于水的CaCO3写成了CO
H2O+CO2↑就是错的。错在将难溶于水的CaCO3写成了CO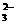 ,正确离子方程式应当是CaCO3+2H+
,正确离子方程式应当是CaCO3+2H+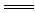 Ca2++H2O+CO2↑。
Ca2++H2O+CO2↑。
③必须遵守质量守恒定律。有人将Na2CO3与稀硫酸反应的离子方程式写成了CO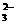 +H2O+CO2↑,因为方程式两边氢原子的个数不相等,所以是错误的,正确的应当是CO
+H2O+CO2↑,因为方程式两边氢原子的个数不相等,所以是错误的,正确的应当是CO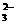 +2H+
+2H+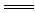 H2O+CO2↑
H2O+CO2↑
④必须遵守电荷平衡原理。如:铝与稀硫酸反应:A1+2H+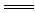 Al3++H2↑(错误),正确的是:2A1+6H+
Al3++H2↑(错误),正确的是:2A1+6H+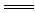 2Al3++3H2↑
2Al3++3H2↑
⑤必须符合阴、阳离子的个数配比。如:氢氧化钡和硫酸溶液反应:
错误:Ba2++OH-+H++SO
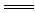 BaSO4↓+H2O,不符合离子的个数配比,一个Ba2+结合的OH-有2个,两个H+对应一个SO
BaSO4↓+H2O,不符合离子的个数配比,一个Ba2+结合的OH-有2个,两个H+对应一个SO 。 正确:Ba2++2OH-+2H++SO
。 正确:Ba2++2OH-+2H++SO
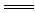 BaSO4↓+2H2O
BaSO4↓+2H2O
20(7分).取一定量的Na2CO3和Na2SO4混合物溶液与过量盐酸反应,生成2.016 L CO2(STP),然后加入足量的Ba(OH)2溶液,得到沉淀的质量为2.33 g。试计算混合物中Na2CO3和Na2SO4的物质的量分别为多少。
知识盘点
1.在水溶液中或熔融状态下能够导电的化合物称为电解质,若是在以上两种情况下都不导电的化合物则称为非电解质。酸、碱、盐在水溶液中能够导电,是因为它们在溶液中发生了电离,产生了能够自由移动的离子。因此,电离是电解质溶液导电的前提。但能导电的物质不一定是电解质,如石墨、铜等;电解质本身不一定能导电,如食盐晶体。
酸、碱、盐等电解质在水溶液中的电离过程可用电离方程式表示,如:H2SO4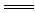 2H++SO
2H++SO ,Ba(OH)2
,Ba(OH)2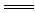 Ba2++2OH-,KNO3
Ba2++2OH-,KNO3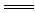 K++NO
K++NO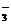 等。电解质溶液的导电能力取决于在相同条件下单位体积内自由移动的离子的数目及其所带电荷的多少。在电解质溶液中,阳离子所带正电荷总数与阴离子所带负电荷的总数是相等的,故溶液显电中性,称电荷守恒。因为电解质溶于水后电离出离子,所以电解质在溶液中的反应必然有离子参加。
等。电解质溶液的导电能力取决于在相同条件下单位体积内自由移动的离子的数目及其所带电荷的多少。在电解质溶液中,阳离子所带正电荷总数与阴离子所带负电荷的总数是相等的,故溶液显电中性,称电荷守恒。因为电解质溶于水后电离出离子,所以电解质在溶液中的反应必然有离子参加。
22.写出下列物质电离方程式:
NaHSO4 ; NaHCO3
21.(2001广东、河南卷18)(7分)甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。回答下面问题:
(1)写出丁与乙反应的离子方程式: 。
(2)这四种溶液分别是甲: 、乙: 、丙: 、丁: 。
20. 现有①硫酸镁 ②硝酸钡 ③氢氧化钠 ④氯化铜 ⑤氯化钾等五种溶液。不加任何试剂即可鉴别,则鉴别的先后顺序是 。 。
19.(14分)某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH- 、NO3- 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子 、 、 。 乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量 (选填:活性炭或铁粉),可以发生 反应,离子方程式是 ,并且能够回收其中的金属 (填写金属元素符号)。
(2)将甲乙两厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式:
;
。
经过滤后的废水主要含 ,可用来浇灌农田。
18.(16分)四只试剂瓶中分别盛装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。
在四支试管中分别取四种溶液各1mL,做下列实验。
(1)在四支试管中分别滴入 ,出现 现象的是 ,
离子方程式是 。
(2)在剩余三支试管中分别滴入 ,出现 现象的是 ,
离子方程式是 。
(3)在剩余两支试管中分别滴入 ,出现 现象的是 ,
离子方程式是 。
三次实验中都没有明显现象的是 。
17.(5分)电解质是指在 和 下能够导电的 。电解质导电的根本原因在于它在这种状态下能够 出自由移动的离子。科学家从这个角度对化合物进行了分类,根据这种分类,酸、碱、盐应该属于 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com