
题目列表(包括答案和解析)
1.下列气体所含原子数最多的是A
A.10g 氨 B.14g 氮气 C.4g 氦气 D.24g 臭氧
26.(附加题,10分)已知:A、B、D、E为四种短周期元素,它们的核电荷数A<B<D<E;A与B可生成共价化合物AB2,每个AB2分子中含有22个电子;D元素与A元素为同主族元素,E元素原子的最外层电子数比次外层少1个。试回答下列下列问题:
(1)写出AB2的电子式 ;
(2)写出A与E形成的共价化合物的结构式_____________ ;
(3)写出E-的结构示意图 ;
(4)D元素和B元素也能形成DB2型共价化合物,但它与AB2相比,在物理性质却有着巨大反差。请你从结构上给予合理的解释 。
25.(6分)某金属重2.4 g,其原子核外有1.2 mol 电子,核内共有7.224×1023个中子,该金属与足量盐酸反应,有0.2 mol电子发生转移,生成了6.02×1022个阳离子。
(1)该金属元素符号是____________,摩尔质量是____________。
(2)原子核内有________个质子,________个中子。
(3)写出该金属与盐酸反应生成的氯化物的电子式 。
24.(10分)下表列出了前20号元素中的某些元素性质的有关数据:
|
元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
|
原子半径(10-10m) |
1.52 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
0.71 |
|
最高价态 |
+1 |
+1 |
- |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
- |
|
最低价态 |
- |
- |
-2 |
- |
-4 |
-3 |
-1 |
- |
-3 |
-1 |
试回答下列问题:
(1)以上10种元素的原子中,最容易失去电子的是 (填写编号);与H2最容易化合的非金属单质是 (写物质名称)。
(2)写出元素③形成的氢化物的电子式_____________________________;
(3)写出上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式 。某元素R的原子半径为1.02×10-10m,该元素在周期表中位于 。
(4)写出④的最高价氧化物的水化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式___________________________________;________________________________。
23.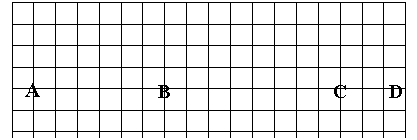 (8分)下图是元素周期表的框架图,请根据下面提问回答:
(8分)下图是元素周期表的框架图,请根据下面提问回答:
(1)在上面元素周期表中全部是金属元素的区域为
① A ② B ③ C ④ D
(2)在短周期元素中,请用化学式填写,与水反应最剧烈的金属元素是 ;元素的气态氢化物最稳定的物质是 ;元素的最高价氧化物所对应的碱其碱性最强的物质是 ;元素的最高价氧化物的水化物中酸性最强的是 。
(3)用物质的名称填写,硬度最大的是单质是 。
(4)短周期中,原子半径最大的非金属元素的原子是 (填写化学式)。
22.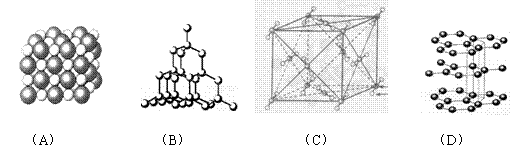 (10分)如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
(10分)如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
(1)其中代表金刚石的是(填编号字母,下同) ,金刚石属于 晶体。
(2)其中代表石墨的是 ,其晶体中碳原子呈平面 结构排列。
(3)其中代表NaCl的是 ,晶体中Na+与Cl-之间通过 键结合起来。
(4)代表干冰的是 ,它属于 晶体,CO2分子间通过 结合起来。
(5)上述物质中前三种熔点由高到低的排列顺序为 。
21.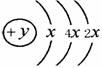 (6分)A、B、C、D四种短周期元素,且A、B、D为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3 和BC2 ,A的原子结构示意图右图,据此填空:
(6分)A、B、C、D四种短周期元素,且A、B、D为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3 和BC2 ,A的原子结构示意图右图,据此填空:
(1)A的元素名称为 ,其气态氢化物的化学式为 。
(2)A、B、C、D四种元素的原子,半径由小到大的顺序为 。
(3)B和D最高价氧化物的水化物化学式分别为 和 。
20.根据化学反应的实质是旧键断裂、新键形成的观点,下列变化没有发生化学键断裂的是 A.电解水 B.干冰受热直接变成气体 C.HCl溶解于水 D.打雷放电时,O2变成O3
第Ⅱ卷 (非选择题 共40分)
19.要使下列物质(①金刚石、②食盐、③干冰、④水晶、⑤金属铝)熔化,需要克服微粒间的相互作用,其中克服的相互作用属于同种类型的是 A.①④ B.②③ C.③④ D.①⑤
18.含有共价键的分子晶体是 A.NaOH B.SiO2 C.Cl2 D.NH4Cl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com