
题目列表(包括答案和解析)
15.为探究原电池的形成条件和反应原理,某同学设计了如下实验步骤并记录了现象:
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述稀硫酸中插入铜片,没有看到有气泡生成;
③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;
④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,正确的是
A.实验①、②说明锌能与稀硫酸反应而铜不能
B.实验③说明发生原电池反应时会加快化学反应速率
C.实验③说明在该条件下铜可以与稀硫酸反应生成氢气
D.实验④说明该原电池中锌为正极、铜为负极
14.能在无色溶液中能大量共存的一组离子是
A.Mg2+、SO42-、OH-、K+ B.Cu2+、NO3-、Cl-、H+
C.H+、Na+、Cl-、SO42- D.K+、OH-、Cl-、NH4+
13.下列离子方程式的书写正确的是
A.钠和水反应
2Na+2H2O 2Na++2OH-+H2↑
2Na++2OH-+H2↑
B.氯气溶于水
Cl2+H2O 2H++Cl-+ClO-
2H++Cl-+ClO-
C.铝和氢氧化钠溶液反应 Al+2OH- AlO2-+H2↑
AlO2-+H2↑
D.铁和氯化铁反应 Fe+Fe3+ 2Fe2+
2Fe2+
12.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.0.36 g水中所含中子数一定为0.2 NA
B.4.48 L N2与CO的混合物所含分子数一定为0.2 NA
C.6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA
D.标准状况下,2.24 L氧气所含原子数一定为0.2 NA
11.下列物质中既含有离子键又含有共价键的是
A.NaOH B.NaCl C.H2O D.NH4Cl
10.可以鉴别LiCl、Na2CO3和KNO3三种无色溶液的方法是
A.分别加入CaCl2溶液 B.分别加入AgNO3溶液
C.分别加入HCl溶液 D.分别做焰色反应实验
9.通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提高生活质量。下列各图所示的措施中,能加快化学反应速率的是
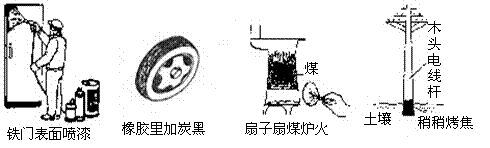
A B C D
8.下列关于浓硫酸的叙述正确的是
A.浓硫酸在常温下能够使铁、铝等金属钝化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸具有吸水性,因而能使蔗糖炭化
7.下列表示物质结构的化学用语中,错误的是
A.10个中子的氧原子的核素符号: B.CO2分子的结构式:O=C=O
B.CO2分子的结构式:O=C=O
C.Cl-离子的结构示意图: D.N2的电子式:
D.N2的电子式:
6.SiO2在室温下不与水、稀盐酸、稀硫酸和稀硝酸等作用,但易溶于氢氟酸,你认为其原因可能是
A.氢氟酸的酸性比其它酸强 B.氢氟酸的氧化性比其它酸强
C.氢氟酸的还原性比其它酸强 D.硅原子极易与氟原子结合
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com